Gracias por apuntarte al webinar
Gracias por registrarse en nuestro seminario web. A medida que se acerque la fecha del seminario web, nos aseguraremos de enviarle más información. ¿Sediento de conocimiento? Mientras tanto, asegúrese de explorar nuestros artículos sobre Life Sciences a continuación.
VALIDACIÓN DE SISTEMAS INFORMATIZADOS: REQUISITOS DE USUARIO (URS)
¿Qué son los Requisitos de Usuario? Los Requisitos de Usuario (RU´s o URS en inglés) son las expectativas que una organización tiene con respecto al
Redacción técnica: la importancia, reglas
Imagínate explicándole el uso de Excel y todas sus funciones a alguien que nunca ha trabajado con el programa en un manual escrito. ¿Por dónde

¿Qué es el desmantelamiento en CSV?
En CSV, el desmantelamiento es la retirada o el cierre controlado de una solución informática o de un sistema informático que ya no es necesario. Conozca más sobre este proceso aquí.

¿Cómo utilizar la firma electrónica en los sectores regulados?
Durante la pandemia, la firma electrónica adquirió una enorme importancia para las empresas del sector regulado. Conozca más sobre la firma electrónica, su uso y su seguridad aquí.

Migración de datos en CSV: definición, propósito y mejores prácticas
A veces es necesario realizar una migración de datos en sistemas informáticos, aplicaciones o software. Conozca más sobre el objetivo, la importancia y los riesgos aquí.

La importancia de las redes de distribución de gas de alta calidad para los gases de proceso críticos, incluso en la fase inicial de desarrollo
La calidad de los gases de proceso y de las redes de distribución de gases es cada vez más importante para los procesos farmacéuticos biotecnológicos y los centros ATMP. En este blog, destacamos la importancia de una red cualificada de gas de proceso y distribución, incluso en una fase temprana de desarrollo.

Control Estadístico de Procesos
Este artículo se enfoca en el control estadístico de procesos y su importancia en la gestión de calidad empresarial, ofreciendo información sobre su implementación, herramientas y métodos, y destacando la relevancia del análisis de datos para la mejora continua.

Proceso y requisitos de validación de la limpieza
Según las GMP’s todas las etapas de fabricación de un medicamento, incluida su limpieza, deben estar validadas para asegurar que el producto sea eficaz, seguro y de calidad, y que cumple con las especificaciones y normativas aplicables.
La limpieza debe considerarse como un paso más en la fabricación de un medicamento, ya que garantiza la calidad de los productos fabricados. El proceso de limpieza reduce los residuos hasta un nivel mínimo aceptable para que no suponga un riesgo para el paciente, ya que se considera que el residuo cero, es casi imposible.

¿Para qué sirven las revisiones periódicas en CSV?
¿Has validado ya tus sistemas informáticos? Entonces, las revisiones periódicas del CSV es el siguiente paso. En este blog te contamos todo sobre las revisiones periódicas en CSV: su propósito, el proceso a seguir y la frecuencia en la que se deben realizar.
La EMA publica la lista negra de GMP
Cuando una instalación de GMP aprobada por las inspecciones de la FDA tenga problemas de incumplimiento, se le notificarán las medidas y los requisitos necesarios
Novedades en el ámbito de las GMP de la EMA (1)
Nuevo Capítulo 2 Personal La EMA no ha dejado de lado los últimos meses en lo que se refiere a su sistema de GMP. El
Novedades en el ámbito de las prácticas correctas de fabricación de la EMA (2)
Archivo maestro de sustancias activas Los pacientes conocen el DMF, o Drug Master File, un documento en el que se proporciona toda la información sobre
Farmacopea japonesa y normas GMP
Para que pueda ver: la farmacopea japonesa y las normas GMP están disponibles en línea en el sitio web de la PMDA (Agencia de Productos
Productos combinados
La FDA publica un proyecto de guía «Buenas prácticas de fabricación actuales: Requisito para productos combinados«. En este momento, la revisión está pendiente, hasta el
Buenas prácticas de distribución (GDP)
USP ha publicado en su página web 5 borradores de artículos, entre ellos las Buenas Prácticas de Distribución (GDP) https://www.usp.org/usp-nf/notices/additional-feedback-sought-proposed-storage-and-distribution-general-chapters. Estos objetivos se basan en
Directriz armonizada para las impurezas elementales
A finales del año pasado, la ICH publicó la directriz armonizada sobre impurezas elementales. Esta directriz establece las PDE (Exposiciones Diarias Permitidas) de los elementos
Proyecto de documento sobre las nuevas orientaciones de la EMA para los importadores de medicamentos
Dado que, con el paso del tiempo, los medicamentos destinados al mercado europeo se producen cada vez más fuera de Europa, la EMA quiere redactar
Alta calidad, bajos riesgos: cómo optimizar la gestión del control de calidad farmacéutico y médico
El pasado mes de marzo, la Unión Europea publicó unas directrices actualizadas en el Eudralex – Volumen 4: Directrices sobre buenas prácticas de fabricación (GMP).
El pie de la QbD en la puerta
A principios de este mes, un equipo de QbD visitó las Jornadas Nórdicas de Ciencias de la Vida en Estocolmo (Suecia). El evento habría estado
Vacunar: ¿un nuevo papel clave para los farmacéuticos?
Con la llegada del invierno, ha llegado el momento de vacunarse contra la gripe. Muchas personas, a menudo mayores de sesenta años o con una
QbD en Estados Unidos: trabajar duro, jugar duro
«Opuestos»: esa es la palabra que me viene a la mente al recordar mi aventura de cuatro semanas de QbD en Estados Unidos. Extremos opuestos.
HistoGeneX elige Quality by Design para garantizar la calidad
QbD apoya el fuerte crecimiento de HistoGeneX optimizando los sistemas informáticos HistoGeneX recurre a la ayuda de Quality by Design, experto en garantía de calidad
Industria farmacéutica: el cumplimiento no siempre equivale a la calidad
Cuando se dice farmacia, se dice cumplimiento. La introducción de nuevos productos farmacéuticos en el mercado está sujeta a normas muy estrictas sobre el desarrollo,
Pruebas de aceptación en fábrica: no es un asunto sencillo
A principios de noviembre de 2015, emprendí un viaje de diez días a Escandinavia. ¿Propósito principal del viaje? Comprobación de una máquina de llenado y
Errores en la producción farmacéutica: por qué las multas no son la solución
45.000 euros. Es la multa que tienen que pagar las empresas farmacéuticas cuando no pueden suministrar inesperadamente ciertos medicamentos. La ministra holandesa de Salud Pública,
Nuevo avance en las negociaciones sobre medicamentos huérfanos
Los últimos avances en el mercado de los medicamentos huérfanos son prometedores. Además de los Países Bajos y Luxemburgo, la ministra flamenca de Salud Pública,
El brillante futuro de la industria belga de las ciencias de la vida
En los últimos tres años, la industria de las ciencias de la vida ha creado entre 3.000 y 3.500 puestos de trabajo adicionales en Bélgica.
Farmacia y automatización en Japón y Bélgica: las diferencias
Como ingeniero de proyectos farmacéuticos en QbD, cada día es diferente. Más aún cuando se visita un país muy diferente al nuestro. El mes pasado
¿Está preparado para las nuevas normas de la FDA y la UE sobre productos sanitarios?
Dos directrices recientes de la FDA En 2016, la Administración de Alimentos y Medicamentos de los Estados Unidos publicó dos documentos de orientación muy diferentes
Ecos de una formación sobre QbD: el poder de Lean
Las formaciones especializadas son una manera de seguir invirtiendo en la experiencia de nuestro equipo de QbD. Tres colegas de QbD comparten sus opiniones sobre

Prepararse para los crecientes retos de la serialización farmacéutica
La serialización está surgiendo rápidamente en el mundo farmacéutico. Para luchar contra la falsificación de medicamentos, cada vez más gobiernos exigen que cada producto de
Digitalizar la sanidad paso a paso
En un mundo cada vez más digital, el entorno sanitario se enfrenta a complejos retos. Está claro que las empresas sanitarias tendrán que adoptar sistemas
Nuevas medidas de la FDA y la UE para eliminar las dobles inspecciones de medicamentos
El Acuerdo de Reconocimiento Mutuo entre Estados Unidos y la Unión Europea está entrando en vigor gradualmente. Desde noviembre de 2017 la FDA reconoce a
Nuevas medidas de la FDA y la UE para eliminar las dobles inspecciones de medicamentos
El Acuerdo de Reconocimiento Mutuo entre Estados Unidos y la Unión Europea está entrando en vigor gradualmente. Desde noviembre de 2017 la FDA reconoce a
¿Qué son las buenas prácticas de distribución?
No hace falta preguntarle a Papá Noel por el PIB. Pregúntale a Sofie. El PIB cubre la crucial «última milla» después de la producción. Es
Nuevo borrador del Anexo 1 de las GMP de la UE
Han pasado más de 10 años desde la última revisión del anexo 1 de las PCF de la UE. El 20 de diciembre de 2017,
La MHPRA del Reino Unido publica las directrices sobre la integridad de los datos GxP
Recientemente, la MHPRA (Agencia Reguladora de Medicamentos y Productos Sanitarios) del Reino Unido publicó un documento de orientación sobre la integridad de los datos en

Actualización de la Buena Práctica Clínica E6(R2)
Cada día, pacientes de todo el mundo participan en ensayos clínicos. Sus contribuciones son cruciales, ya que garantizan el progreso de una investigación vital. Sin
Garantizar la plena integridad de los datos, sin excepciones
La integridad de los datos es la piedra angular del progreso científico. Sin embargo, un reciente artículo publicado en un importante periódico belga muestra que
Retos y oportunidades en el panorama de los dispositivos médicos
El panorama de los productos sanitarios está sometido a normas y reglamentos cada vez más estrictos. Aunque a veces se perciba como una molestia, lo
Una mirada crítica al nuevo borrador del Anexo 1 de las BPF de la UE
El 20 de diciembre de 2017, la Agencia Europeade Medicamentos (EMA) publicó el borrador para el nuevo Anexo 1 de BPF de la UE «Fabricación
¿Gestión de la calidad en otros sectores? ¡Comprobado!
Por supuesto, es fundamental que las empresas de ciencias de la vida cumplan las normas de calidad más estrictas. Pero muchos otros sectores también están
Pioneros con Inteligencia Artificial para hacer más accesible la terapia celular personalizada
Varios avances científicos y clínicos de nuestra última década demuestran que los medicamentos de terapia avanzada (ATMP) revolucionarán la medicina del siglo XXI. Utilizando células
Nuestra sanidad y la impresión en 3D: ¿una combinación perfecta?
En los últimos años, las técnicas de impresión en 3D han revolucionado el sector sanitario en todo el mundo. La impresión 3D tiene la capacidad
La revolución de la impresión 3D en Terapias Avanzadas.
En los últimos años, las técnicas de impresión 3D han revolucionado la industria de la salud en todo el mundo. La impresión 3D tiene la
Regulación de la MDR y falta de coordinación de los implantes: Mejoras a realizar
Estos últimos días, la falta de regulación de los dispositivos médicos (MDR) en la Unión Europea ha sido destacada por muchos medios de comunicación. Como
Legislación sobre productos sanitarios: cómo estar al día
El 26 de septiembre de 2012, la Comisión Europea adoptó una propuesta de reglamento del Parlamento Europeo y del Consejo, para revisar la legislación existente

La integridad de los datos en la industria farmacéutica: una breve introducción
En los últimos dos años, el tema de la integridad de los datos ha recibido cada vez más atención. Recientemente, la Administración de Alimentos y

Antleron y QbD se alían para crear un desprendimiento en la sanidad
Cada día está más cerca una nueva era en la asistencia sanitaria. Gracias al cruce de Con la impresión 3D y la biología, las soluciones
Dispositivos médicos: una amplia categoría para innumerables aplicaciones vitales
Los productos sanitarios desempeñan literalmente un papel vital en la sociedad. Como son clave para curar a los pacientes y salvar vidas, están sujetos a

Anexo I de las BPF de la UE: ¿Estamos preparados para los retos que se plantean tras su revisión?
Tras meses de revisión y muchas preguntas planteadas, parece que ha llegado el momento de aplicar los nuevos requisitos contenidos en la revisión del anexo

La serialización en la UE puede convertirse en una ventaja competitiva si se atreve a innovar
La falsificación siempre ha sido un problema importante. Aunque puede parecer un buen negocio cuando se puede encontrar su marca favorita de bienes de consumo
Un día en la vida de QbD de… Henrik, consultor de cumplimiento de QA
¿Quiere saber cómo es un día típico de trabajo en Quality by Design? En la primera parte de nuestro nuevoSerie de blogs «Un día en

Sudando la tristeza del lunes
Cómo la QbD pone el «juego» en el «trabajo, juego, entrega» – parte 1 Hace tiempo, Martijn, uno de los socios gestores de QbD, tenía

Un día en la vida de … Imrane, ingeniero de procesos
¿Se pregunta cómo es un día típico de trabajo en Quality by Design? En la segunda parte de nuestra serie de blogs «Un día en
Introducción en el mercado de nuevos productos sanitarios: ¿presentarlos bajo la MDD o la MDR?
Los países dependen del uso de dispositivos médicos para lograr la cobertura sanitaria universal, responder a las emergencias sanitarias y mantener la seguridad de la

Validación de procesos como punto focal para la cualificación y validación del centro de competencia
El grupo de calificación y validación dentro de QbD organizó su primera Centro de Competencia hace unas semanas. Este foro se utiliza para debatir temas

Escritura técnica: la importancia, lo que hay que hacer y lo que no hay que hacer
Imagina que le explicas el uso de Excel y todas sus funciones a alguien que nunca ha trabajado con el programa, en un manual escrito.

Bélgica, pionera en materia de medicamentos antirretrovirales: ahora y en el futuro
Respaldado por las crecientes inversiones de los patrocinadores comerciales, el desarrollo de medicamentos de terapia avanzada (ATMP) está creciendo con fuerza en el Reino Unido.

Un día en la vida de QbD de… Lieve, experta en procesos downstream en eTheRNA immunotherapies
¡Es hora de invadir la privacidad de otro QbDer! En su «Día en la vida de QbD de…», Lieve De Wolf nos acerca a un

Cómo lucha Europa contra los medicamentos falsificados
La fabricación y venta de medicamentos es un gran negocio. En consecuencia, los medicamentos falsificados son una grave amenaza para los pacientes que dependen de

Un día en la vida del QbD de… Evelyne, farmacéutica y persona cualificada y responsable
sta semana, la farmacéutica Evelyne Goudezeune nos trae un típico «Día en la vida de la QbD», lleno de varias reuniones y una velada muy entretenida. ¿Te gusta lo que lees? Entonces asegúrate de enviarnos tu cv para unirte a nuestro increíble equipo

Cuidado con el Ejército Rosa
La QbD es conocida por su espíritu de equipo y su carácter deportivo. Esto no sólo ocurre en la oficina, sino también fuera del trabajo.

Un día en la vida de QbD de… Julie, socia de RRHH en QbD HQ
Ha llegado el momento de echar un vistazo al día a día de otro de nuestros QbD’s. Conoce a Julie Bondroit, una de las integrantes
La salida al mercado de las vacunas: La Unión Europea frente a los Estados Unidos de América
Cuando se trata de la salida al mercado de las vacunas, hay algunos requisitos y legislaciones específicas que las empresas deben tener en cuenta. En esta entrada del blog, prestaremos atención a la salida al mercado de las vacunas en dos de los mercados más importantes del mundo: la Unión Europea y los Estados Unidos de América. Aunque son bastante similares, hay algunas diferencias interesantes en lo que respecta a las pruebas, la documentación y la certificación.

¿Cómo afectará el Brexit a la industria farmacéutica de la Unión Europea?
El reloj está en marcha para el Brexit. Antes del 31 de octubre de 2019, debe alcanzarse un acuerdo definitivo al respecto. No cabe duda de que la salida del Reino Unido de la Unión Europea (UE) tendrá un enorme impacto en el Reino Unido y en los Estados miembros de la UE.

Un día en la vida de QbD de… Jolien, consultor farmacéutico
Como Ingeniero de Apoyo a la Producción doy soporte a mi cliente Biocartis con problemas asociados al proceso de producción. Dependiendo del problema, mi trabajo

La inteligencia artificial en los medicamentos de terapia avanzada
Los medicamentos de terapia avanzada (ATMP) son terapias celulares y genéticas que ofrecen nuevas oportunidades para el tratamiento de diversas enfermedades y lesiones. Debido a

Del QMS a la validación: QbD enseña a los futuros ingenieros biomédicos en Lieja
Allí estábamos, en el «quartier Polytech», buscando el departamento «Aérospatiale & Mécanique» de la universidad de Lieja. Nos habíamos levantado demasiado temprano, pero una pequeña

Sudando la tristeza del lunes: ¡esta vez vía livestream!
Como saben, QbD es una organización muy deportiva y saludable. Como hoy empieza la semana 2 de deberes y distanciamiento social, obviamente echamos de menos
Conferencias RA/QA en la Universidad de Lieja – semana 2
El siguiente episodio del programa de conferencias invitadas para los estudiantes de Ingeniería Biomédica de la Universidad de Lieja fue una nueva experiencia tanto para
Todo lo que necesita saber sobre los ATMP: FAQ
¿Cuál es la definición de ATMP? Del sitio web de la EMA: Los medicamentos de terapia avanzada (MTA) son medicamentos de uso humano basados en

Un día en la vida de QbD de… Frederick Tison – Corona times
¡Hola! Mi nombre es Frederick Tison. Tengo 26 años y este es mi tercer año en QbD. Actualmente estoy activo como especialista en materias primas
Un día en la vida de… nuestro equipo de contratación de QbD
Mientras se apliquen las medidas COVID-19, el equipo de contratación de QbD seguirá trabajando desde casa. Pero gracias a la tecnología moderna y a nuestra

Conferencias invitadas de RA/QA – semana 3 – Hoja de ruta para el marcado CE
(Este blog forma parte de una serie. ¿Quieres leer la primera parte? Compruébelo aquí) Después de las vacaciones de Semana Santa, QbD reanudó sus conferencias

Conferencias invitadas de RA/QA – semana 4 – Software como dispositivo médico y Calificación y Validación
El lunes 27 de abril, los estudiantes de Ingeniería Biomédica de la Universidad de Lieja asistieron a la cuarta conferencia invitada de QbD. En esta ocasión, Bart Verlinden y Pieter Smits, responsables de QbD, introdujeron a los estudiantes en el software como dispositivo médico y en la validación y cualificación.
Conferencias invitadas de RA/QA – semana 5 – FDA y Dispositivos Médicos
El 4 de mayo, le tocó a Maaike Tuinsma (consultora farmacéutica de QbD) dar una conferencia a los estudiantes de Ingeniería Biomédica de la Universidad de Lieja. Tema de esta semana: La FDA y los productos sanitarios.

Empezar un nuevo trabajo en tiempos de Corona: así lo vivió Katrien en QbD
¿Una congelación de la contratación durante Corona? ¡No puede ser! Aunque la crisis actual ha creado nuevos e inesperados retos, QbD no es el tipo
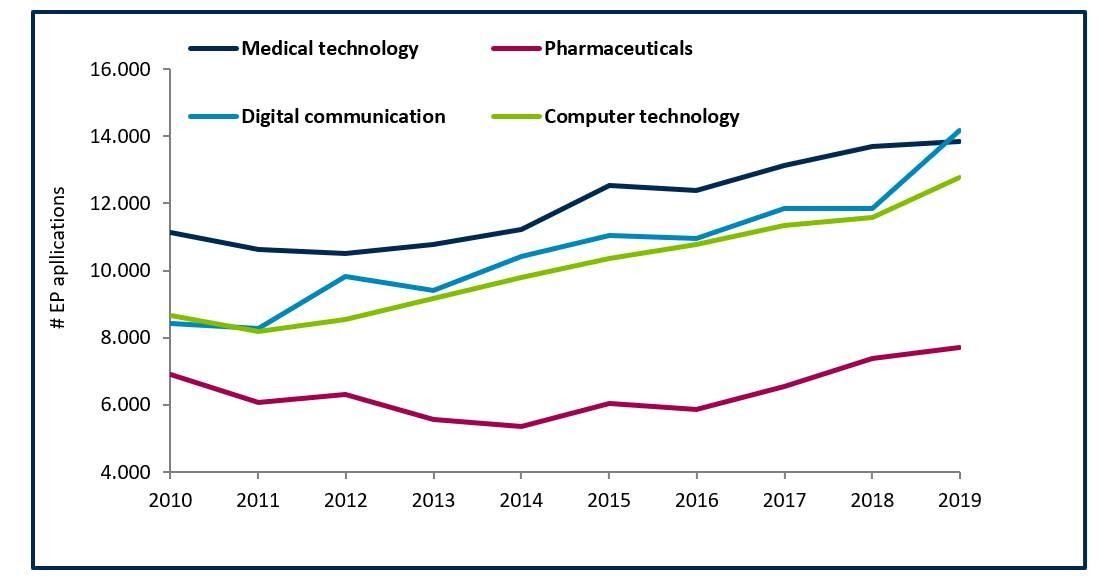
Innovaciones en tecnología médica: El futuro de la sanidad son los datos
La innovación es la clave del éxito de las empresas y es el motor de muchas industrias. Esto es ciertamente cierto para el sector de

Desarrollo de mascarillas en la lucha contra la pandemia de COVID-19
Este blogpost pretende proporcionar información útil para las partes implicadas en el desarrollo de mascarillas en la lucha contra la pandemia de COVID-19. Enumera el

Estos factores pueden hacer que la transferencia de tecnología sea un éxito o un fracaso
Una transferencia de tecnología puede tener lugar entre edificios del mismo centro de producción, entre diferentes plantas de producción de la misma empresa o incluso

Transferencias tecnológicas: ¿cuáles son los motores de la complejidad?
En este blogpost, nos adentraremos un poco más en estas complejidades y le daremos algunos consejos útiles para minimizar la complejidad de sus transferencias tecnológicas.

¿Cómo empezar con la validación del sistema informático?
Las empresas de ciencias de la vida, por ejemplo, de la industria farmacéutica, biotecnológica y de dispositivos médicos, deben validar los sistemas informáticos que repercuten

La importancia de un equipo dedicado y un director de proyecto capacitado para las transferencias de tecnología
¿Ha leído nuestros anteriores artículos del blog sobre los factores que pueden hacer que su transferencia de tecnología sea un éxito o un fracaso, y los factores de complejidad en las transferencias de tecnología?

El uso de wearables en el diagnóstico y la prevención de enfermedades
¿Comprobando su teléfono para ver cuándo tomó su última medicación? ¿Su reloj vibrando y diciéndole que se acueste porque va a tener un ataque pronto, mientras que al mismo tiempo notifica a su contacto de emergencia con su ubicación exacta?

En qué se debe centrar la validación de un sistema informático
En el primer blog hablamos de las definiciones de validación y sistemas informáticos. La comprobación de la aptitud del sistema consiste en verificar si el sistema funciona de acuerdo con las necesidades del proceso para el que se adquiere.

Fabricación de ATMP para el mercado: principales obstáculos que hay que superar para garantizar un producto final de alta calidad.
Hasta ahora, el mundo académico y las empresas basadas en la investigación han sido la principal fuente de desarrollos exitosos de ATMP (terapia génica y productos de ingeniería celular o tisular). Basándose en su éxito, las empresas farmacéuticas están intentando

Tres importantes tendencias en la transferencia de tecnología
¿Ha leído nuestras anteriores publicaciones en el blog sobre la importancia de un equipo dedicado y un gestor de proyectos cualificado para las transferencias de tecnología, los factores que pueden hacer que su transferencia de tecnología sea un éxito o un fracaso y los factores de complejidad en las transferencias de tecnología?

¿En qué hay que fijarse para validar un sistema informático? (2)
En el primer blog hablamos de las definiciones de validación y sistemas informáticos. La comprobación de la aptitud del sistema consiste en verificar si el sistema funciona de acuerdo con las necesidades del proceso para el que se adquiere.
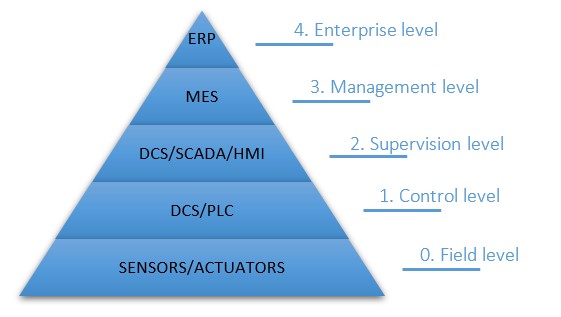
Pirámide de automatización – Preguntas frecuentes
¿Qué implica una pirámide de automatización? Una pirámide de automatización visualiza las capas integradas de tecnología utilizadas en la fabricación o la industria, combinadas con
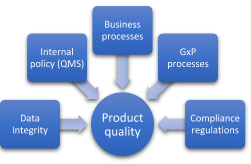
¿En qué hay que fijarse para validar un sistema informático? (3)
Procesos GxP Sin duda, el impacto de los procesos de GxP, como la calidad de los productos y la salud de los pacientes, ocupan el
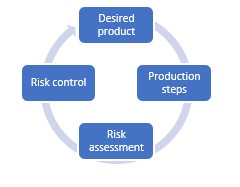
Metodología de calidad por diseño para la industria farmacéutica
Es obvio que la calidad de los productos y la seguridad de los pacientes son una prioridad absoluta en la industria farmacéutica. La metodología de
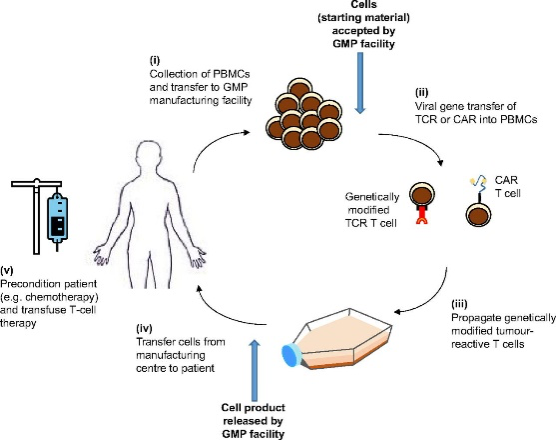
CAR T y TCRs para el mercado: estado actual y perspectivas de futuro
Entre los medicamentos de terapia avanzada (ATMP), en el mercado de la inmunoterapia, hoy en día dos siglas llaman la atención: CAR-T y TCR-T. Las

Conozca a nuestro nuevo socio TRIUM Clinical Consulting: entrevista con el Director General Christof Debèfve
Recientemente hemos anunciado que Quality by Design y TRIUM Clinical Consulting han unido sus fuerzas para crear una oferta integral para el ciclo de vida
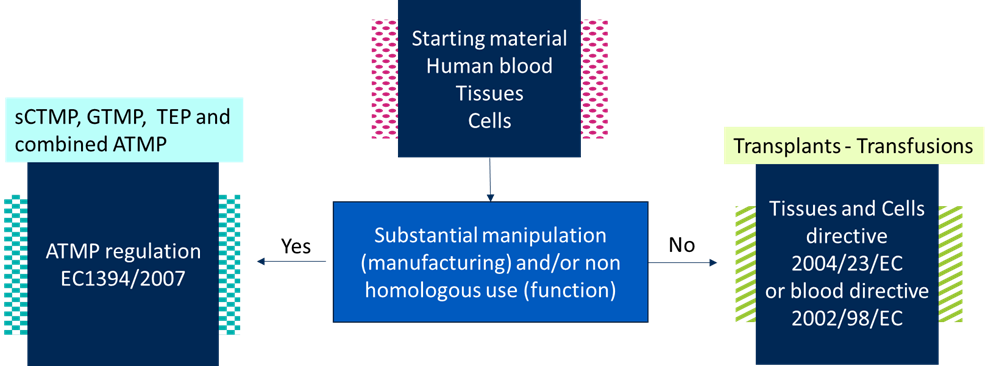
¿Es su plataforma ATMP lo suficientemente robusta como para hacer frente a la variabilidad de los materiales?
¿Quiere distinguir los materiales de partida utilizados para los ATMP de los utilizados para los trasplantes o las transfusiones? Esta distinción se hace en función

Productos sanitarios: innovaciones frente a normativas
Uno de nuestros anteriores artículos del blog hablaba de las innovaciones en el campo de la tecnología médica y de cómo éstas pueden satisfacer las

Vigilancia postcomercialización de productos sanitarios
Breve introducción y resumen de los requisitos En 2017, la Comisión Europea publicó el nuevo Reglamento de Productos Sanitarios (MDR) que sustituirá a la Directiva

Los Juegos Mundiales Corona – Una vuelta de tuerca del equipo ganador
Durante los QbD Corona World Games, nuestro evento internacional de formación de equipos en línea, trece equipos seleccionados al azar defendieron su honor.
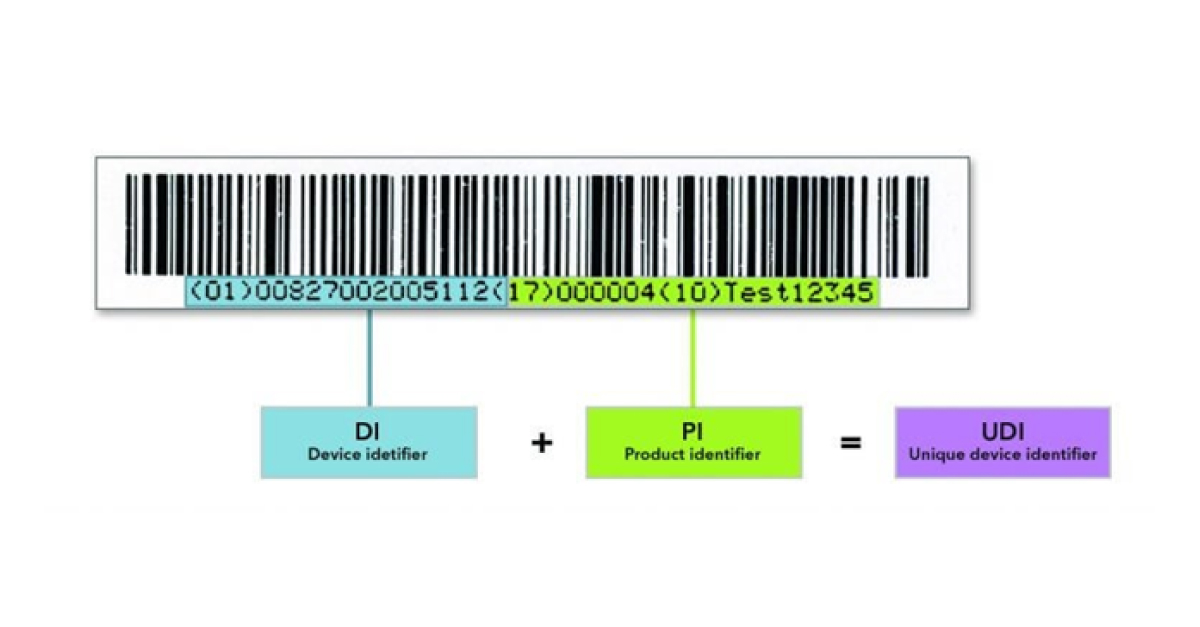
Lo que necesita saber para que su dispositivo médico esté listo a tiempo para el UDI
UDI es un nuevo sistema que asigna un código de barras único a cada producto sanitario. Será obligatorio cuando entren en vigor el MDR y el IVDR, por lo que, como fabricante, debe asegurarse de estar preparado para la UDI a tiempo.

¿Cómo se reduce el coste de los productos, que es la clave para que los medicamentos de terapia avanzada sean asequibles?
El precio de venta de las terapias celulares y génicas está influido por múltiples factores como el coste de los productos (COG), los requisitos normativos, el mercado objetivo (o aspecto comercial) y el desarrollo, por citar algunos. En esta entrada del blog aprenderá más sobre el aspecto GOC: ¿de qué se compone este coste y cómo puede reducirlo?
Aquí encontrará artículos y noticias interesantes relacionados con su sector.