.png?width=1600&height=900&name=Hero%20image%20(6).png)
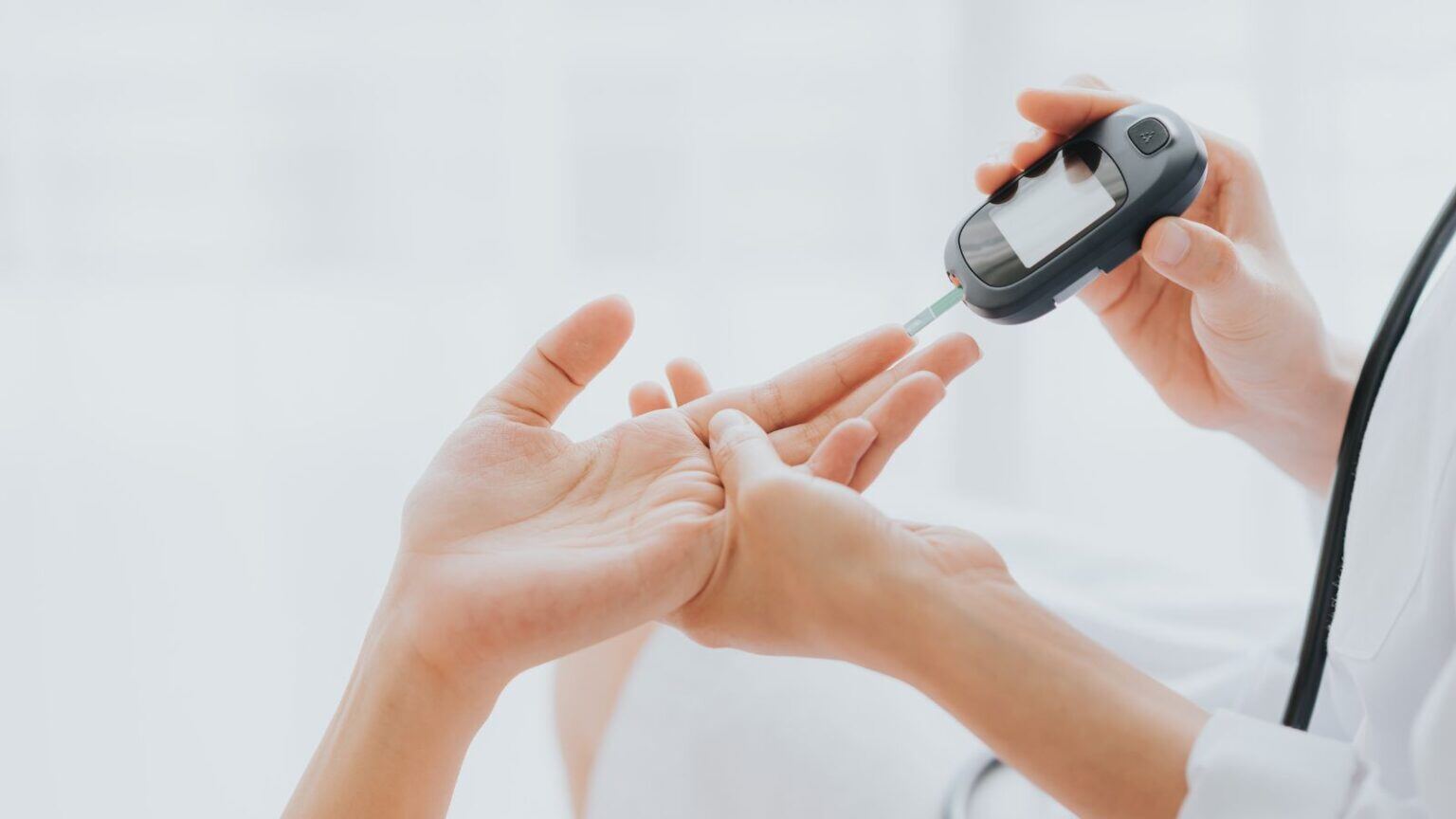
Recursos
Explora nuestros recursos para acceder a información experta en el campo de life sciences. Aquí encontrarás una amplia variedad de contenido, que incluye informes técnicos detallados, artículos de blog, casos de estudios, webinars y actualizaciones normativas.
Ya sea que trabajas en Pharma, Biotech, Medical Devices o cualquier otro sector, nuestros diversos servicios y la orientación de nuestros expertos están diseñados para mantenerte informado y a la última de las tendencias del sector. Descubre nuestro contenido y mantente al día con los avances más recientes y las prácticas más óptimas.
Ya sea que trabajas en Pharma, Biotech, Medical Devices o cualquier otro sector, nuestros diversos servicios y la orientación de nuestros expertos están diseñados para mantenerte informado y a la última de las tendencias del sector. Descubre nuestro contenido y mantente al día con los avances más recientes y las prácticas más óptimas.
All
Blog
Case study
Regulatory update
Webinar
Whitepaper
All Industry
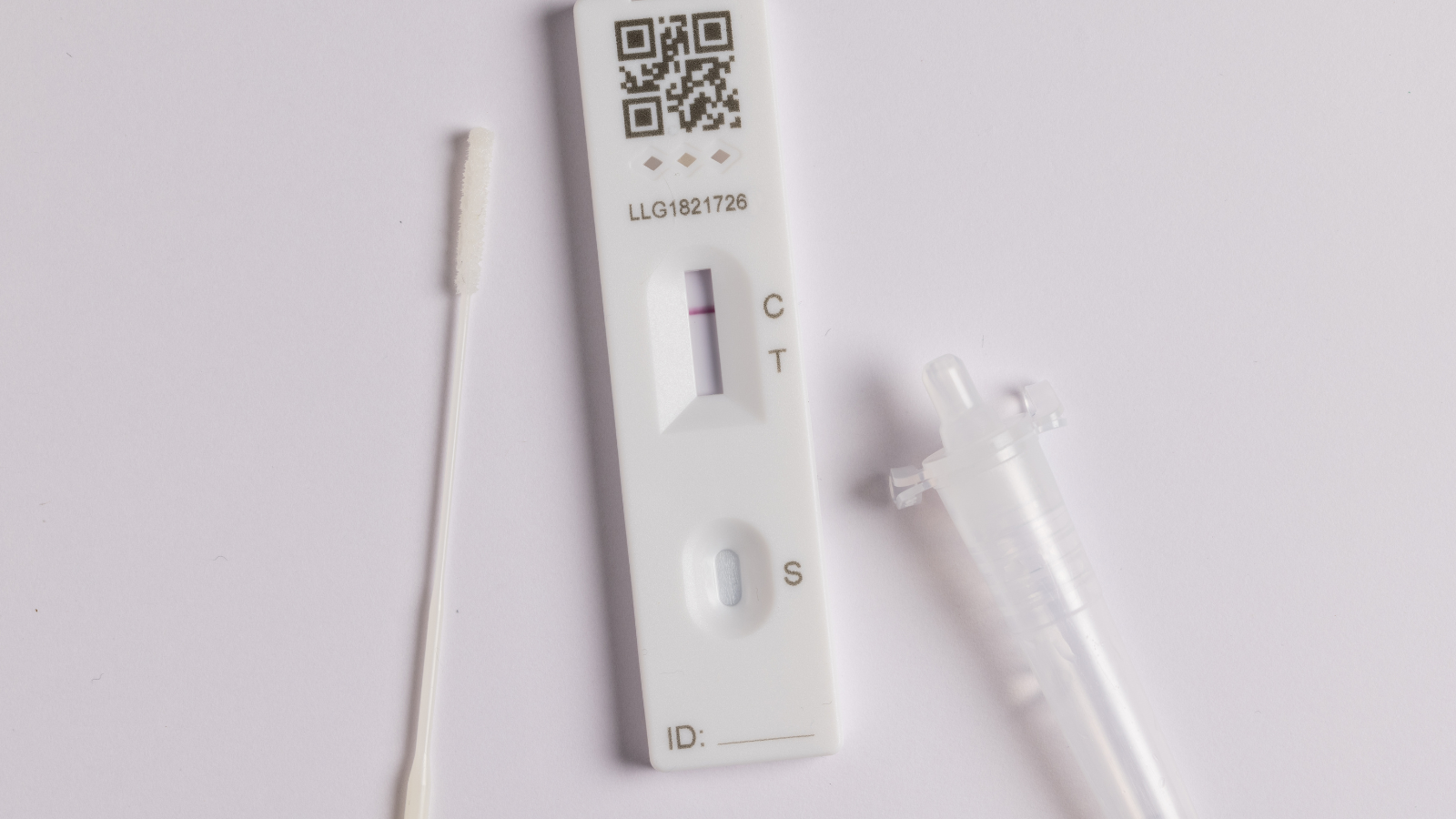
In Vitro Diagnostics
Medical Devices
Pharma & Biotech
All Service
Quality Assurance
Clinical
Lab Services
Qualification & Validation
Vigilance
Regulatory Affairs
Software Solutions & Services
Toxicology
Filter
All
Blog
Case study
Regulatory update
Webinar
Whitepaper
All industries
In Vitro Diagnostics
Medical Devices
Pharma & Biotech
All services
Quality Assurance
Clinical
Lab Services
Qualification & Validation
Vigilance
Regulatory Affairs
Software Solutions & Services
Toxicology

Whitepaper
16 sep 2024
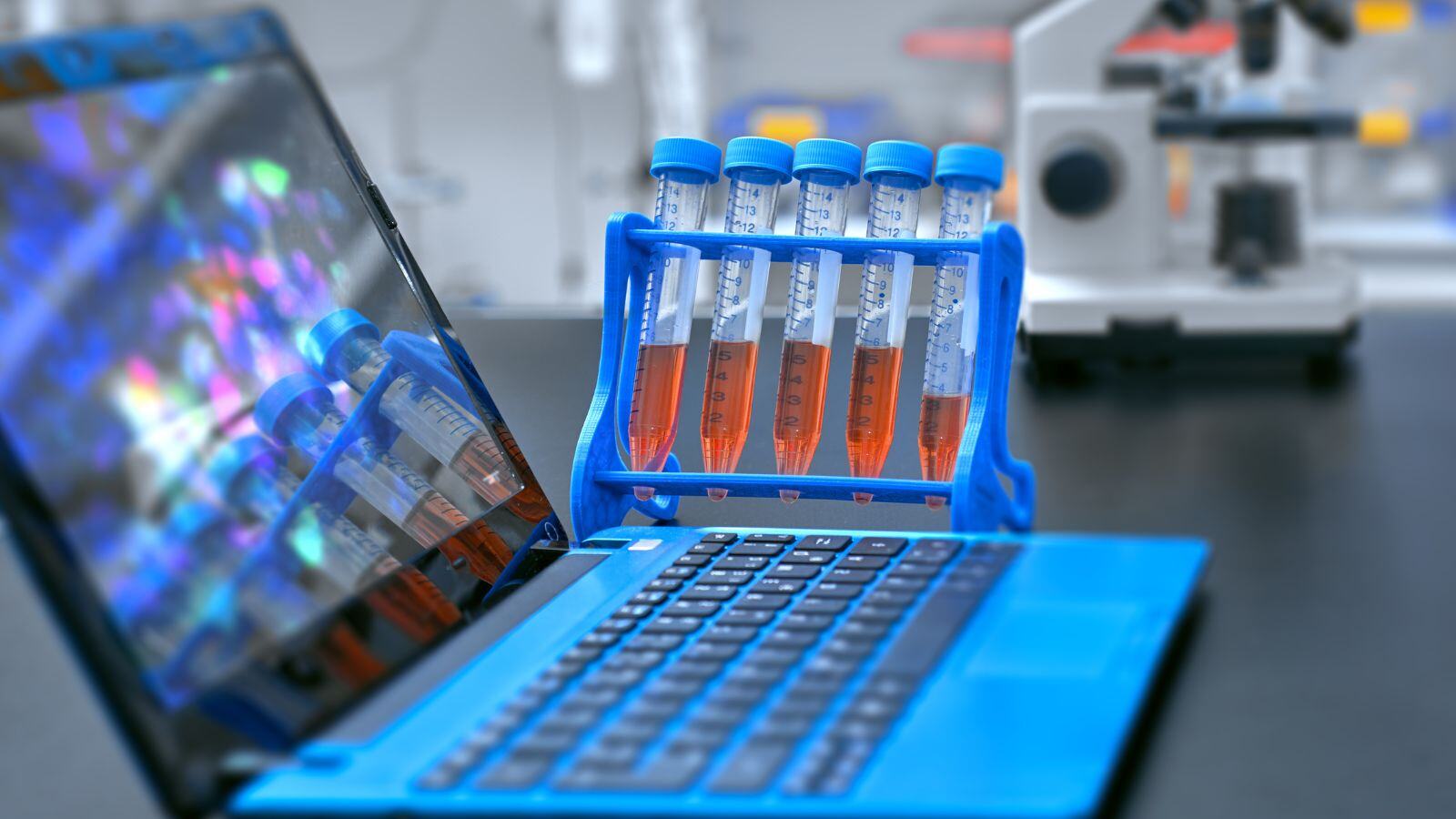
Del modelo V al Agile: cómo adoptar la automatización en la validación de sistemas computarizados
Este whitepaper explora el cambio hacia Agile en IT, con un enfoque en la metodología Scrum y concluye con orientación sobre cómo adaptar los procesos de validación de sistemas.
Leer más

Whitepaper
23 dic 2024
Revisión bibliográfica de última generación: inicia la evaluación clínica de tu dispositivo médico
Este whitepaper te guiará paso a paso en la realización de búsquedas bibliográficas sistemáticas sólidas para la evaluación clínica de tu dispositivo médico. Descárgalo ahora.
Leer más

Whitepaper
8 oct 2024
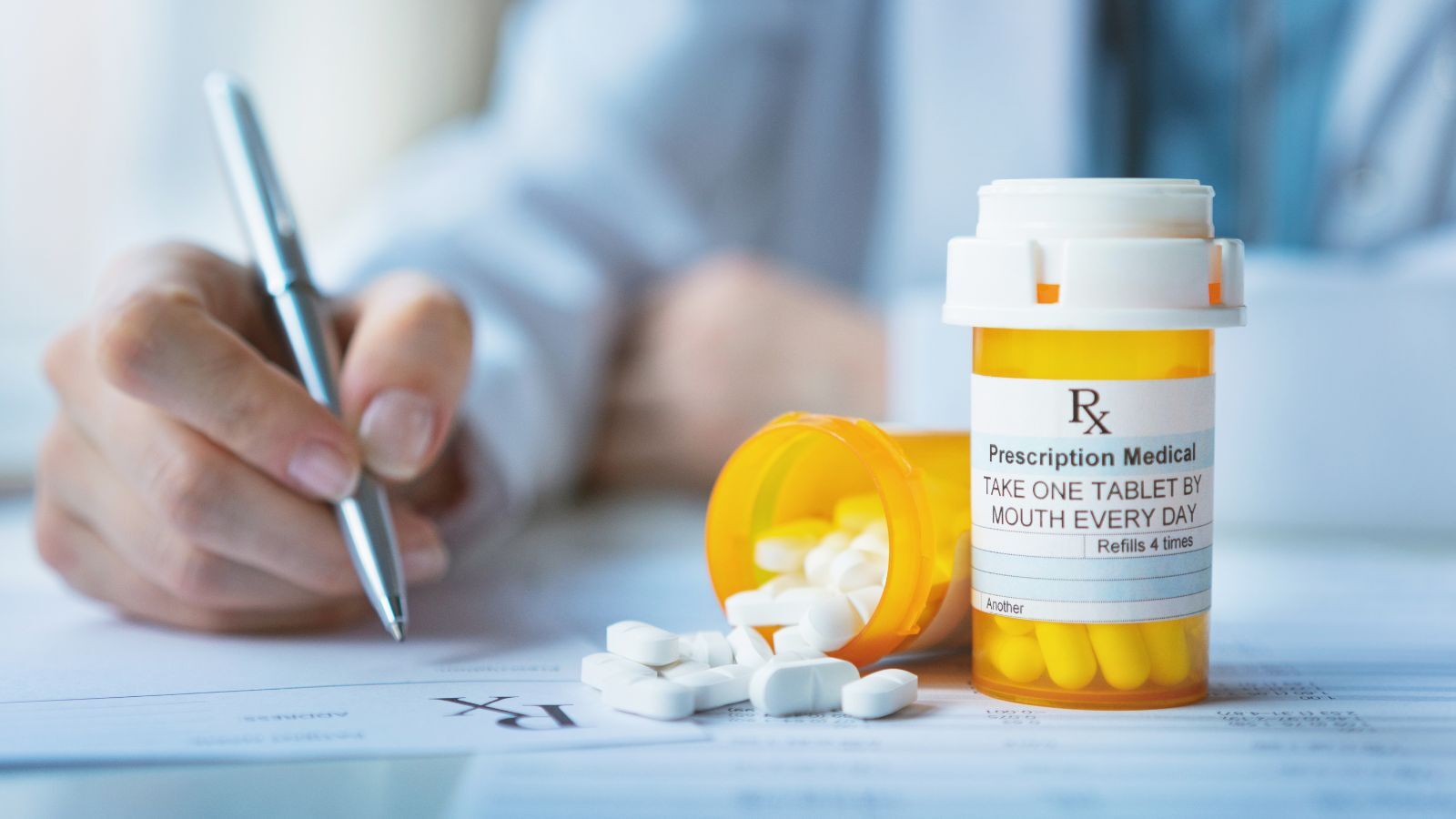
El papel clave de Asuntos Regulatorios en la industria farmacéutica: desde el desarrollo hasta la comercialización
Descubre el papel clave de los Asuntos Regulatorios en la industria farmacéutica y cómo los equipos de Regulatory Affairs apoyan la gestión del ciclo de vida del producto.
Leer más

Case study
25 mar 2024
Garantizar una transición fluida de los productos sanitarios de Oystershell al MDR
El panorama de las normativas sobre productos sanitarios evoluciona constantemente, lo que supone un reto para las empresas mantenerse al día. Nuestra colaboración con Oystershell, que comenzó en...
Leer más
.png)
Case study
31 may 2024
Garantizar la calidad de la producción farmacéutica: validación de la limpieza para una agencia gubernamental
Descubra cómo QbD Group ayudó a un cliente a afrontar los retos de la doble validación de sus líneas de producción, garantizando el cumplimiento de las GMP y la aprobación de la AEMPS.
Leer más

Case study
27 jun 2024
Garantizar el lanzamiento a tiempo: El papel del Grupo QbD en la creación de una línea de producción de medicamentos para la hemofilia
QbD Group ha facilitado la puesta en marcha de una nueva línea de producción de fármacos para el tratamiento de la hemofilia, supervisando la cualificación de más de 100 equipos de apoyo a pequeña...
Leer más
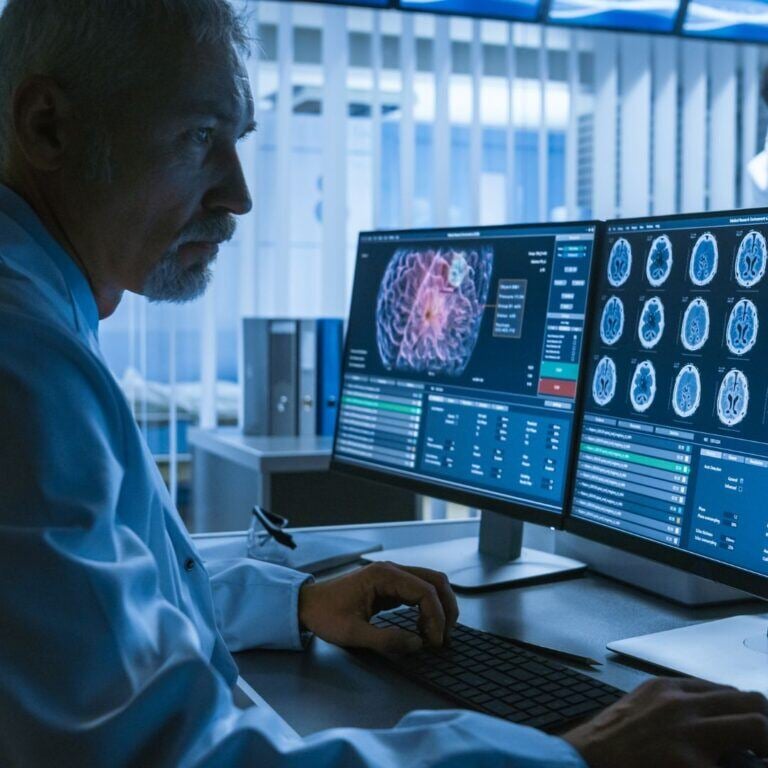
Case study
30 oct 2024
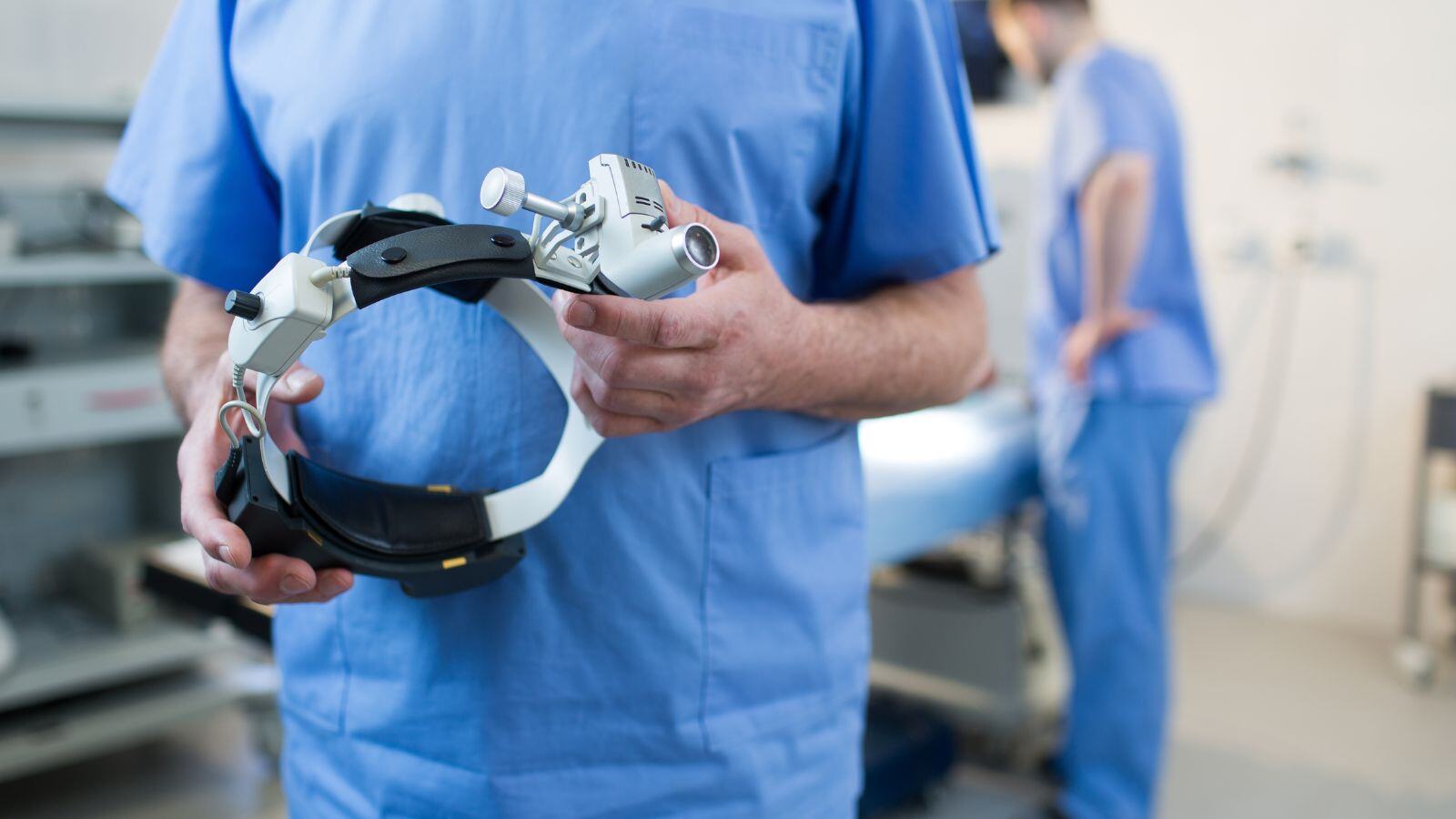
Guiar la investigación del glioblastoma de la Universidad Católica de Lovaina hacia la clínica con una planificación empresarial precisa
Ayudamos a la Universidad Católica de Lovaina a trasladar la investigación sobre el glioblastoma a la clínica con planificación empresarial estratégica, apoyo financiero y una hoja de ruta para el...
Leer más

Case study
28 jun 2024
Optimización de la farmacovigilancia para una empresa líder en biotecnología
Ayudamos a la Universidad Católica de Lovaina a trasladar la investigación sobre el glioblastoma a la clínica con planificación empresarial estratégica, apoyo financiero y una hoja de ruta para el...
Leer más

Case study
31 may 2024
Revolucionando la farmacovigilancia: una historia de éxito de asociación estratégica e integración sin fisuras
Descubra cómo el apoyo experto de QbD Group mejoró la farmacovigilancia de una empresa farmacéutica, lo que condujo a un resultado de inspección favorable por parte de la Autoridad Reguladora local...
Leer más

Webinar
9 ene 2025
Evidencia a lo largo del ciclo de vida: integrando necesidades clínicas en diseño y documentación
Aprende cómo integrar las necesidades clínicas en el diseño de software para dispositivos médicos y cumplir con los requisitos de MDR. Visualiza ahora nuestro webinar bajo demanda.
Leer más

Webinar
Recording
6 ene 2025
De los requisitos al código: un ciclo de desarrollo unificado para software de dispositivos médicos
Aprende sobre el desarrollo de software para dispositivos médicos, incluidos los estándares IEC, ciberseguridad, integración de IA y expectativas de la FDA en este webinar.
Leer más

Webinar
24 dic 2024
Del concepto al mercado: estrategias integrales de acceso al mercado para software de dispositivos médicos
Descubre cómo lanzar con éxito el software para dispositivos médicos, con conocimientos clave sobre estrategias de acceso al mercado y comercialización. Visualiza ahora nuestro webinar.
Leer más
.jpg)
Webinar
19 nov 2024
Primeros pasos: superando obstáculos iniciales en el desarrollo de software para dispositivos médicos
Supera los obstáculos iniciales en el desarrollo de software para dispositivos médicos y en el cumplimiento con MDR, IA Act y mejores prácticas. Visualiza ahora nuestro webinar.
Leer más
.jpg)
Webinar
8 dic 2024
Desbloqueando el valor estratégico en la seguridad de medicamentos para organizaciones de ciencias de la vida
Descubre cómo los equipos de seguridad farmacológica pueden transformarse en impulsores proactivos de beneficios con las herramientas y recursos adecuados en este webinar bajo demanda.
Leer más

Webinar
13 feb 2025
Bases de datos de seguridad en Farmacovigilancia: ¿Cuál es su importancia estratégica?
13 de febrero | 16:00 CET |Descubre la importancia de las bases de datos de seguridad en farmacovigilancia y mejora tu gestión de eventos adversos en nuestro próximo webinar. ¡Regístrate ahora!
Leer más
Webinar
20 feb 2025
El uso de la IA en Farmacovigilancia: gestión de ICSRs y otras aplicaciones clave
20 de febrero | 16:00 CET | Descubre en nuestro próximo webinar cómo la IA transforma la farmacovigilancia, optimizando la detección de eventos adversos y mejorando la seguridad del paciente....
Leer más
Webinar
27 feb 2025
Transformando consultas en insights: el rol estratégico de los Medical Call Centers en Pharma
27 de febrero | 16:00 CET | Descubre cómo los Medical Call Centers transforman consultas en insights estratégicos en la industria farmacéutica en nuestro próximo webinar. Regístrate ahora y aprende...
Leer más
Case study
1 abr 2025
Una década de excelencia: soporte en revisión lingüística para un líder farmacéutico global.
QbD Group optimiza las revisiones lingüísticas para un cliente farmacéutico líder, garantizando cumplimiento y precisión en 25 idiomas de la UE/EEE, cumpliendo con estrictos plazos regulatorios.
Leer más

Webinar
13 may 2025
De la evaluación al cumplimiento: guía práctica sobre el riesgo de las nitrosaminas
Descubre cómo gestionar el riesgo de las nitrosaminas en la industria farmacéutica en nuestro webinar. Inscríbete y aprende de la mano de expertos todo sobre regulaciones y el análisis de riesgo.
Leer más

Case study
28 may 2025
Validación de una carga de autoclave compleja para optimizar la eficiencia de la esterilización
Descubre cómo QbD Group ayudó a una planta farmacéutica de Barcelona a optimizar y validar una compleja carga de autoclave, mejorando la eficacia de la esterilización y la flexibilidad de la...
Leer más

Blog
27 jun 2025
La farmacovigilancia es una responsabilidad compartida: Por qué la notificación de eventos adversos es más importante que nunca
Descubre cómo los profesionales sanitarios y los pacientes contribuyen a la seguridad de los medicamentos informando sobre acontecimientos adversos: una parte...
Leer más

Blog
27 may 2025
El papel de las Buenas Prácticas de Distribución (GDP) y de la Gestión del Riesgo de Calidad (QRM) para garantizar la integridad farmacéutica
Descubre cómo las Buenas Prácticas de Distribución (GDP) y la Gestión de Riesgos de Calidad (QRM) garantizan la integridad, seguridad y cumplimiento de los...
Leer más

Blog
7 may 2025
Una planificación y gestión más inteligente de las auditorías en life sciences: cumplir la normativa y ahorrar tiempo
Mejora la planificación, ejecución y seguimiento de auditorías en life sciences con un enfoque estructurado y basado en el riesgo — además de cuándo y por qué...
Leer más

Blog
25 abr 2025
La importancia de las auditorías de farmacovigilancia veterinaria: Protegiendo la salud global cumpliendo con las normativas vigentes
Las auditorías de farmacovigilancia veterinaria son fundamentales para la salud global. Descubre cómo QbD te ayuda a cumplir con las VGVP y garantizar la...
Leer más

Blog
5 mar 2025
Container Closure Integrity Testing (CCIT) en la Industria Farmacéutica: Garantizando la seguridad de los envases farmacéuticos.
Aprende cómo las Container Closure Integrity Testing (CCIT) en la Industria Farmacéutica protegenlos envases farmacéuticos, garantizando la esterilidad,...
Leer más

Blog
13 feb 2025
Revisión del anexo 1 de las GMP de la UE: Fabricación de medicamentos estériles - Resumen y primeras impresiones
En 2022 se revisó el Anexo 1 de las GMP de la UE, Fabricación de medicamentos estériles. En esta entrada del blog, proporcionaremos un resumen de los cambios y...
Leer más

Blog
25 sep 2024
Mantener la excelencia en la validación: Mejora continua mediante revisiones periódicas de la validación en la Industria Farmacéutica
Aprende cómo las revisiones periódicas de validación mantienen la conformidad del sistema farmacéutico, utilizando el análisis basado en el riesgo y la...
Leer más

Blog
18 sep 2024
La Tecnovigilancia en acción: Protegiendo la salud con la vigilancia postcomercialización de los productos sanitarios
Descubre cómo la tecnovigilancia garantiza la seguridad de los dispositivos médicos a través de la vigilancia post-comercialización, abordando los principales...
Leer más

Blog
16 sep 2024
Externalización de los procesos de conocimiento en la seguridad de los medicamentos: Una externalización más inteligente para una asistencia sanitaria más segura
Descubre cómo la externalización estratégica de procesos de conocimiento (KPO) está revolucionando los departamentos de seguridad de los medicamentos...
Leer más

Blog
4 sep 2024
Dominio de la información sobre productos de la EU: el papel del proceso de revisión lingüística de la EMA en los procedimientos centralizados
Obtén información esencial sobre el proceso de revisión lingüística de la EMA de la información de producto de los medicamentos aprobados mediante el...
Leer más

Blog
19 abr 2024
Evaluaciones de riesgos medioambientales (ERA) en la industria farmacéutica: equilibrio entre salud y medio ambiente - QbD Group
Explore how Environmental Risk Assessment (ERA) helps ensure medicines heal us without harming the planet, balancing healthcare advances with ecological...
Leer más

Blog
5 dic 2023
Procedimiento de reconocimiento internacional de la MHRA tras el Brexit: navegando por el registro de medicamentos en el Reino Unido
Explora el nuevo Procedimiento de Reconocimiento Internacional (IRP) de la MHRA para medicamentos posteriores al Brexit y aprende a navegar por las...
Leer más

Blog
7 jul 2023
Diseño de cámaras climáticas o de estabilidad conforme a las GMP: la clave para garantizar la integridad del producto
En esta entrada del blog, nos adentramos en el mundo del diseño de cámaras climáticas que cumple con las GMP y desentraña el papel vital que desempeñan en las...
Leer más

Blog
1 sep 2022
Colabora con una organización de investigación por contrato (CRO) dedicada a los productos sanitarios para impulsar tu estrategia de investigación clínica.
Descubre 5 razones para contratar a una Organización de Investigación por Contrato (CRO) especializada en estudios de productos sanitarios para apoyar tu...
Leer más

Blog
17 jul 2022
La importancia de las redes de distribución de alta calidad para los gases de proceso críticos, incluso en la fase inicial de desarrollo
La calidad de los gases de proceso y las redes de distribución de gas es cada vez más importante para los procesos farmacéuticos biotecnológicos y los sitios...
Leer más

Blog
25 abr 2021
De la idea a la vigilancia posterior a la comercialización: las fases del ciclo de vida de los productos sanitarios
El lanzamiento de un dispositivo médico requiere mucha preparación. Como estos dispositivos están fuertemente regulados, una empresa tiene que cumplir muchos...
Leer más

Regulatory update
1 jul 2025
Actualización de plazos de la FDA - Riesgo de impureza relacionada con sustancias activas de nitrosaminas (NDSRI)
El 23 de junio de 2025, la FDA publicó una aclaración sobre el próximo plazo del 1 de agosto de 2025 relacionado con las impurezas asociadas a sustancias...
Leer más

Regulatory update
6 mar 2025
Convocatoria de manifestaciones de interés para la evaluación coordinada de investigaciones clínicas/estudios de rendimiento
El 6 de febrero de 2025, los Estados Miembros de la UE y la Comisión Europea anunciaron el lanzamiento de una evaluación piloto coordinada de investigaciones...
Leer más

Regulatory update
18 sep 2024
La FDA publica una revisón de la guía sobre el control de las impurezas de nitrosaminas en medicamentos de uso humano
La FDA acaba de publicar una versión actualizada de su guía sobre el control de las impurezas de nitrosamina en los medicamentos de uso humano, que introduce...
Leer más
 No Blog Post Found!
No Blog Post Found!








.png?width=109&height=108&name=Pharma%20(2).png)




















.jpg)

.jpg)
.jpg)
.png)

.jpg)

.jpg)