Gracias por apuntarte al webinar
Gracias por registrarse en nuestro seminario web. A medida que se acerque la fecha del seminario web, nos aseguraremos de enviarle más información. ¿Sediento de conocimiento? Mientras tanto, asegúrese de explorar nuestros artículos sobre Life Sciences a continuación.

Externalización de los procesos de conocimiento en la seguridad de los medicamentos: Una externalización más inteligente para una asistencia sanitaria más segura
Descubre cómo la externalización estratégica de procesos de conocimiento (KPO) está revolucionando los departamentos de seguridad de los medicamentos farmacéuticos, impulsando la eficiencia y la innovación.

Adelántate al Cumplimiento: Cómo gestionar eficazmente tus auditorías anuales
Gestiona las auditorías anuales para garantizar el cumplimiento y la calidad en la industia farmacéutica y en el sector de productos sanitarios. ¡Aprende estrategias clave para mejorar tu SGC!

Importancia de la Validación de Hojas de Cálculo en Entornos Regulados
En la actualidad, las hojas de cálculo son herramientas esenciales para una variedad de tareas, desde la contabilidad y el análisis de datos hasta la planificación y la gestión de proyectos. Sin embargo, en industrias altamente reguladas como la farmacéutica, de dispositivos médicos y biotecnología, es crucial que estas herramientas no solo sean eficientes, sino también precisas y conformes a las normativas. Los errores en hojas de cálculo pueden ocurrir con frecuencia, y sus consecuencias en estos sectores pueden ser graves, afectando la integridad de los datos y poniendo en riesgo la seguridad del producto final. La validación de hojas de cálculo garantiza que cumplan con los requisitos de calidad y regulaciones específicas, minimizando el riesgo de errores y asegurando la integridad de los datos.

Garantizando la Calidad del Producto, la Seguridad del Paciente y la Integridad de Datos en la Industria Farmacéutica
La industria farmacéutica es un pilar fundamental en la salud y el bienestar de la sociedad. Detrás de cada medicamento hay un meticuloso proceso de desarrollo, fabricación y distribución, donde la calidad del producto, la seguridad del paciente y la integridad de datos juegan roles críticos. En este blog, exploraremos cómo estas áreas se entrelazan para asegurar la excelencia en los productos farmacéuticos, fundamentales para la salud pública

Buenas Prácticas de Farmacovigilancia: Garantizando la Seguridad de los Medicamentos
La farmacovigilancia es un campo crucial en la industria farmacéutica y en la salud pública en general. Se encarga de la detección, evaluación, comprensión y prevención de los efectos adversos o cualquier otro problema relacionado con el uso de medicamentos. En términos más simples, la farmacovigilancia se centra en reunir información sobre los posibles efectos secundarios de los medicamentos una vez que están en el mercado y en uso. Esto incluye, efectos adversos conocidos y aquellos que no se habían identificado durante los ensayos clínicos antes de la aprobación del medicamento.

¿Por qué tengo que seguir examinando mi SGC según el IVDR si tiene la certificación ISO 13485?
Los fabricantes de IVD deben alinear la ISO 13485 y el IVDR para disponer de un Sistema de Gestión de la Calidad conforme. Este artículo explora las consideraciones clave para armonizar estos marcos.

Éxito de la post-comercialización en el marco del IVDR: dar prioridad al PMS y al PMPF
A medida que el sector del IVD experimenta importantes cambios normativos con la aplicación del Reglamento (UE) 2017/746 (IVDR), los fabricantes se enfrentan a nuevos retos y requisitos en relación con la vigilancia poscomercialización (PMF) y el seguimiento del rendimiento post-comercialización (PMPF). En este artículo, exploramos la importancia de priorizar la PMS y el PMPF en el marco del IVDR.

El papel crucial de las pruebas clínicas en el cumplimiento del IVDR
Este artículo explora la importancia de las pruebas clínicas para los productos sanitarios de diagnóstico in vitro (IVD) según el nuevo Reglamento (UE) 2017/746 de la Unión Europea (IVDR), y los retos a los que se enfrentan los fabricantes para cumplir estos nuevos requisitos.

¿Por qué empezar ahora a elaborar Documentación Técnica conforme al IVDR?
Incluso con la propuesta de la Comisión Europea de ampliar el periodo transitorio para los IVD, los fabricantes deben empezar a elaborar ya una Documentación Técnica conforme. Este artículo destaca la importancia de actuar de forma proactiva a pesar del retraso propuesto.

Comprender la propuesta de la Comisión Europea de ampliar el periodo transitorio para los Diagnóstico In Vitro
La Comisión Europea propone ampliar los plazos para cumplir el nuevo Reglamento sobre productos sanitarios para diagnóstico in vitro (IVDR). Este artículo analiza los motivos de la ampliación y lo que significa para los fabricantes.

Prórroga transitoria del IVDR: Por qué avanzar a toda velocidad sigue siendo la mejor estrategia
Este artículo explora por qué mantenerse en la senda del cumplimiento del IVDR sigue siendo la mejor estrategia para los fabricantes de productos sanitarios.

Friabilidad y Desintegración para Formas de Dosis Sólidas Orales: Las pruebas olvidadas
Descubre el papel crucial de las pruebas de friabilidad y desintegración para garantizar la calidad, seguridad y eficacia de los comprimidos farmacéuticos.

El riesgo de contaminación por benceno en los medicamentos: Lo que deben saber los fabricantes
Infórmate sobre los riesgos de contaminación por benceno en los productos farmacéuticos, las directrices normativas y las mejores prácticas para garantizar la seguridad y la calidad de los medicamentos en la fabricación.
Evaluación Toxicológica de Extraíbles y Lixiviables (EL)
Infórmate sobre los Extraíbles y Lixiviables en los productos farmacéuticos, incluidas las directrices normativas, las técnicas analíticas y las evaluaciones de seguridad.

Comprender los productos sanitarios informáticos: Navegando por la normativa de la UE y las evaluaciones clínicas
Descubre qué se necesita para obtener y mantener la aprobación de comercialización de Productos Sanitarios Software en la UE.
Certificación MDR para dispositivos heredados: Integración de pruebas clínicas para el cumplimiento
Averigua qué se necesita para mantener la autorización de comercialización de dispositivos antiguos en la UE.
Tipos de redacción médica: Introducción al arte de la redacción médica en la sanidad
Exploremos el campo de la redacción médica y los diferentes tipos de proyectos de redacción médica en Sanidad. En QbD Clinical estaremos encantados de ayudarle.

Validación de Sistemas de Monitoreo en la Industria Farmacéutica
En la actualidad, las regulaciones en la industria farmacéutica han llevado a las empresas relacionadas con la salud a mejorar e implementar nuevos procesos en toda la cadena de producción de medicamentos. Esto abarca desde la fabricación de materias primas, la producción de los medicamentos, hasta la logística para su entrega al usuario final.
Entre los procesos nuevos y mejorados, el control y monitoreo de las condiciones ambientales en las áreas de producción y almacenamiento se ha vuelto crucial. Este monitoreo incluye parámetros como la temperatura, la humedad relativa y la presión atmosférica. En este blog, exploraremos la importancia de estos sistemas en la industria farmacéutica, ofreceremos algunos consejos clave para un buen monitoreo y responderemos preguntas frecuentes sobre la validación de estos sistemas.

Entregables para la Validación de un sistema ERP
En el mundo empresarial, la validación de sistemas computarizados es un proceso esencial para asegurar la calidad y el cumplimiento regulatorio. SAP, uno de los sistemas ERP más utilizados, no es la excepción. La validación de SAP implica una serie de pasos y documentación que garantizan que cada módulo funcione correctamente y cumpla con las normativas establecidas. En este blog, exploraremos el proceso de validación de SAP, detallando los entregables necesarios y explicando cada paso.

Artículo 31 Arbitrajes en Farmacovigilancia: Un breve resumen
Infórmate sobre el procedimiento de arbitraje del artículo 31 de la EMA para evaluar la seguridad de los medicamentos y resolver problemas en la UE.

Preparación para la inspección regulatoria: Un enfoque proactivo del CAPA y el cumplimiento
Consejos de preparación para la inspección: Aprende a gestionar las fallas y a mejorar con CAPA para un mejor cumplimiento de la normativa.

Preguntas Frecuentes sobre la Validación de un ERP
En el dinámico mundo empresarial actual, la eficiencia operativa y la integración de procesos son cruciales para asegurar el éxito. Los sistemas de Planificación de Recursos Empresariales (ERP, por sus siglas en inglés) juegan un papel fundamental en este sentido, al centralizar y automatizar las funciones clave de una organización, desde la gestión financiera hasta la cadena de suministro y la producción. Sin embargo, la implementación de un ERP no es una tarea sencilla. Es vital asegurar que el sistema funcione correctamente y cumpla con los requisitos específicos de la empresa, y aquí es donde entra en juego la validación del ERP.
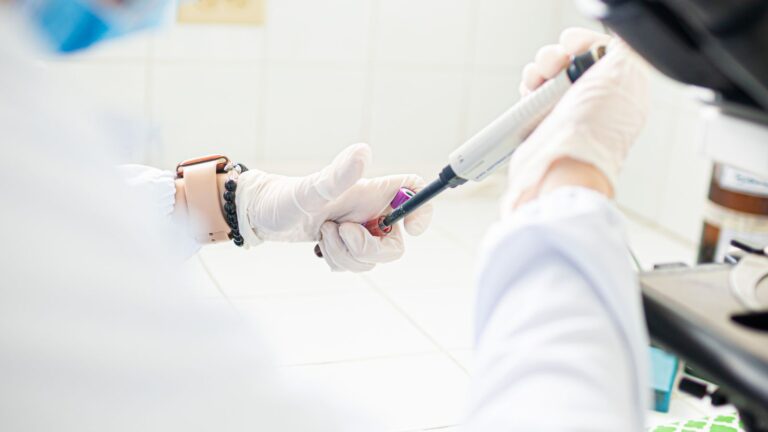
Importancia de las especificaciones de la OMS para la industria farmacéutica
En life sciences, un sector cada vez más digitalizado, la incorporación de nuevas tecnologías además de ayudar a hacer más eficientes los recursos y los procesos, conlleva ciertas implicaciones en cuanto a riesgos que son inherentes a la digitalización de los procesos. Existen diversas razones por las cuales las empresas de life sciences son blanco de ataques cibernéticos y dependen de prácticas sólidas y medidas fuertes de ciberseguridad para protegerse contra las amenazas y garantizar un entorno digital seguro.

Cómo Evaluar y Mejorar la Legibilidad de los Medicamentos: Guía Completa
En el mundo de la medicina, la legibilidad de los medicamentos es un aspecto fundamental para garantizar la seguridad y la compresión por parte de los pacientes. El objetivo de las consultas es asegurar la adecuada interpretación del prospecto por parte de los pacientes o usuarios destinatarios del medicamento. Sin embargo, es preocupante constatar que muchos de los prospectos y etiquetas de medicamentos presentan un nivel de complejidad que dificulta su compresión por la mayoría de las personas. En este blog, exploraremos la importancia de evaluar la legibilidad de los medicamentos de uso humano y los métodos utilizados para medirla.

Transferencia de métodos analíticos: Errores comunes y cómo evitarlos
Descubre los errores habituales en las transferencias de métodos analíticos y aprende estrategias para evitarlos y conseguir procesos de desarrollo y fabricación de fármacos sin fisuras.

Eleva las importaciones farmacéuticas con los Anexos 16 y 21 de las GMP de la UE
Descubre cómo los Anexos 16 y 21 de la GMP de la UE mejoran la calidad y seguridad de las importaciones farmacéuticas. Infórmate sobre su impacto global en la salud pública.

Aplicación de las Normas PIC/S en las Salas Blancas de los Hospitales: De la normativa a la aplicación
Aprende a implantar las normas PIC/S en las salas blancas de los hospitales antes de 2026 para garantizar la calidad, la seguridad y el cumplimiento de los preparados farmacéuticos.

El papel de la inteligencia artificial (IA) en la farmacovigilancia en Europa: Avances y Legislación
Explora el papel transformador de la IA en la farmacovigilancia en Europa, mejorando la seguridad de los medicamentos y el cumplimiento de la normativa de la EMA mediante herramientas avanzadas de IA y legislación.

Las redes sociales en farmacovigilancia: Aprovechar las conversaciones en línea para la seguridad de los medicamentos
Explora cómo las redes sociales ayudan al control de la seguridad de los medicamentos en tiempo real y los retos que plantean en la farmacovigilancia.

Impurezas de nitrosamina en los medicamentos: Riesgos y Normativas
Infórmate sobre las impurezas de las nitrosaminas en los medicamentos, sus causas, las orientaciones normativas y las estrategias de evaluación y mitigación de riesgos.

Una profunda inmersión en las métricas y conclusiones de la inspección de las Buenas Prácticas de Farmacovigilancia (GPvP) de la MHRA
Obtén una visión más profunda de cómo la MHRA inspecciona los servicios de Farmacovigilancia de un MAH para productos post-autorizados.

Cualificación de Salas Blancas: navegando a través de la normativa
Descubre la normativa sobre cualificación de salas blancas, explorando el impacto de las distintas fases de ensayo (cualificación, clasificación, recalificación, supervisión) con especial atención a la evaluación de riesgos.

Automatización SCADA en la industria farmacéutica: aumentando la eficacia y la conformidad
Descubre cómo los sistemas de automatización SCADA incrementan la eficiencia y garantizan el cumplimiento de la normativa en la fabricación de productos farmacéuticos.

Protegiendo a los medicamentos: Control de las impurezas elementales (ICH Q3D)
Explora los riesgos de las impurezas elementales en los medicamentos y cómo la guía ICH Q3D ayuda a garantizar la seguridad y el cumplimiento de los productos.

Impacto de los PDE en el diseño de la validación de la limpieza en la fabricación de productos farmacéuticos
Explora cómo influyen los PDE en la validación de la limpieza en los productos farmacéuticos, garantizando la seguridad y el cumplimiento de las normas del sector.

Garantizar la validación continua de las aplicaciones web y en la nube mediante pruebas automatizadas
Explora cómo las pruebas automatizadas garantizan la validación continua de las aplicaciones web y en la nube, reduciendo los riesgos y optimizando la implantación.
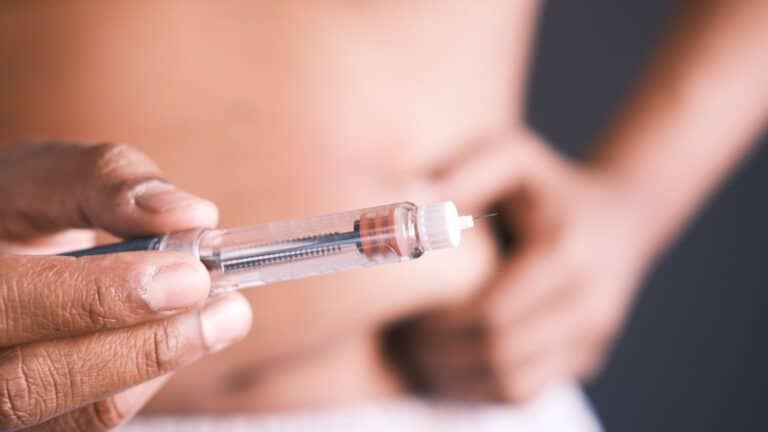
Los productos combinados fármaco-dispositivo y el artículo 117: ¿Cómo cumplir la normativa?
Descubre cómo navegar por el cumplimiento del artículo 117 del MDR para las combinaciones fármaco-dispositivo. Garantiza la correcta aplicación con orientaciones esenciales.

Evaluación de Riesgos Ambientales (ERA) en la Industria Farmacéutica: Equilibrio entre Salud y Medio Ambiente
Explora cómo la Evaluación de Riesgos Medioambientales (ERA) ayuda a garantizar que los medicamentos nos curen sin dañar el planeta, equilibrando los avances en la industria farmacéutica con la preservación ecológica.

Programas de apoyo al paciente: Mejorar la atención al paciente mediante la farmacovigilancia
Descubre cómo los Programas de Apoyo al Paciente (PSP) y la Farmacovigilancia mejoran la atención al paciente, garantizando la seguridad y el cumplimiento durante todo el proceso de atención sanitaria.

ICH Q2(R2) Validación de métodos analíticos: Visión general de la guía revisada
La nueva ICH Q2(R2) es una revisión completa de la guía para incluir una aplicación más reciente de los procedimientos analíticos y alinear el contenido con la ICH Q14 «Desarrollo de procedimientos analíticos».

Cómo evitar la no conformidad en la industria farmacéutica
Este blog subraya la naturaleza crítica del cumplimiento normativo en la industria farmacéutica. Destaca la importancia del compromiso de la alta dirección a pesar de los costes significativos. Se destacan elementos clave como los planes de Acción Preventiva y Correctiva (CAPA), especialmente con la tendencia hacia soluciones informatizadas. La no conformidad puede tener graves consecuencias financieras, por lo que es necesario adoptar medidas proactivas. Los programas de cumplimiento eficaces incluyen procedimientos escritos, personal designado, formación, comunicación y supervisión. El cumplimiento legislativo se considera cada vez más una ventaja estratégica y no sólo una medida de ahorro de costes.

Asegurando la efectividad: Puntos clave para la calificación de autoclaves
¿Qué es una autoclave? Es un recipiente metálico de paredes gruesas con cierre hermético que permite trabajar con vapor de agua a alta presión y

Puntos claves en las etapas del mapeo térmico
El mapeo térmico es una técnica en la cual se utilizan sensores de condiciones ambientales para monitorear y registrar las variaciones en áreas específicas, esta

Celebración del Día Internacional de la Mujer con Elly De Bruyn, CHRO del QbD Group
Para celebrar el Día Internacional de la Mujer, nos sentamos con Elly De Bruyn, Directora de Recursos Humanos del QbD Group, para hablar de sus experiencias y opiniones como mujer poderosa en el sector de las ciencias de la vida.

Auditorías de farmacovigilancia (FV): Importancia, proceso y retos
Conoce el papel crucial que juegan las auditorías de farmacovigilancia (FV) para garantizar la seguridad de los medicamentos y el cumplimiento con la legislación vigente.

Retos de la toxicología en la industria farmacéutica: ¿cómo abordarlos?
Explora cómo afrontar los retos toxicológicos actuales y futuros en la industria farmacéutica, garantizando la seguridad de los productos y la responsabilidad medioambiental.

La ciberseguridad como parte de una estrategia de cumplimiento de integridad de datos GxP
En life sciences, un sector cada vez más digitalizado, la incorporación de nuevas tecnologías además de ayudar a hacer más eficientes los recursos y los procesos, conlleva ciertas implicaciones en cuanto a riesgos que son inherentes a la digitalización de los procesos. Existen diversas razones por las cuales las empresas de life sciences son blanco de ataques cibernéticos y dependen de prácticas sólidas y medidas fuertes de ciberseguridad para protegerse contra las amenazas y garantizar un entorno digital seguro.

MDR Certification for Legacy Devices: Integrating Clinical Evidence for Compliance
Discover what is required to maintain marketing approval for legacy devices in the EU.

Gestión de auditorías de calidad: Auditorías de calidad gestionadas conforme al QMS
Las auditorías GxP son la espina dorsal para cumplir con la legislación y la mejora continua del servicio. Desde la planificación basada en el riesgo hasta la ejecución y la revisión del cumplimiento, en cada paso se garantiza la mejor ejecución. Adoptar una visión del ciclo de vida PDCA (planificar, hacer, comprobar, actuar) para agilizar los procesos y fomenta la coherencia.

Informe 37 de la OMS: Buenas prácticas de manufactura
El Informe 37 de la OMS nos habla sobre las Buenas Prácticas de Manufactura en la industria farmacéutica. Se enfoca en la importancia de mantener estándares de calidad para garantizar la seguridad y eficacia de los medicamentos. Además, proporciona pautas clave como sanitización y validación para cumplir con los requerimientos de auditoría.

Calidad y Asuntos Regulatorios: Elementos clave de un SGC sólido para el cumplimiento y el éxito en farma
Calidad y Asuntos Regulatorios: Descubra los elementos clave de los Sistemas de Gestión de Calidad en la industria farmacéutica para el cumplimiento y el éxito.
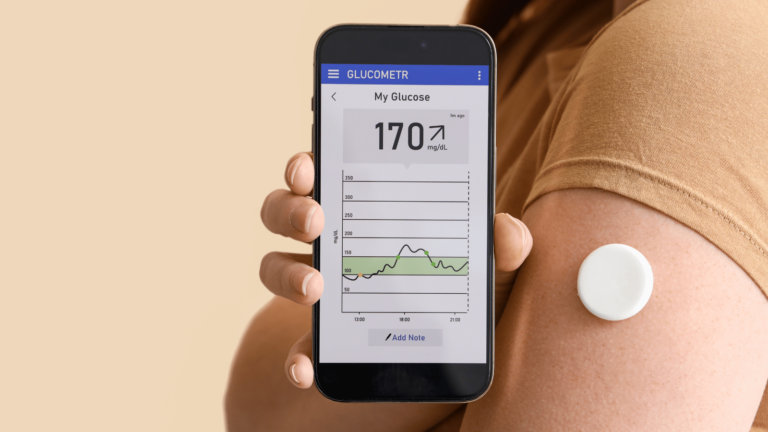
El auge del Mobile Health: Una mirada más atenta al panorama normativo de la UE
Para los fabricantes de DTx dirigidos al mercado europeo, el cumplimiento del reglamento (UE) 2017/745 (MDR) es obligatorio. Profundicemos en este aspecto normativo dentro de la UE.

Validación de métodos analíticos: ¿Son tus métodos analíticos adecuados para el uso previsto?
En este blog, aprenderás más sobre la validación de métodos analíticos y los criterios a tener en cuenta a la hora de validar tu método analítico.

Validación de procesos de limpieza
La validación de procesos de limpieza es crucial en las Buenas Prácticas de Manufactura (BPM) para asegurar la calidad consistente de productos farmacéuticos y prevenir la contaminación.

La ciberseguridad como parte de una estrategia de cumplimiento de integridad de datos GxP
En life sciences, un sector cada vez más digitalizado, la incorporación de nuevas tecnologías además de ayudar a hacer más eficientes los recursos y los procesos, conlleva ciertas implicaciones en cuanto a riesgos que son inherentes a la digitalización de los procesos. Existen diversas razones por las cuales las empresas de life sciences son blanco de ataques cibernéticos y dependen de prácticas sólidas y medidas fuertes de ciberseguridad para protegerse contra las amenazas y garantizar un entorno digital seguro.

Calificación de tanques y marmitas: Un papel fundamental en la producción y procesamiento de productos
En este blog, hablaremos sobre el uso de los tanques en la industria según su tipología y de los documentos claves para su calificación.
Calificación de neveras de cadena de frío: Implementación de protocolos
En este blog, exploraremos la importancia de la cadena de frío y cómo la implementación de estos protocolos puede garantizar la integridad de los productos, así como la confiabilidad del proceso en su totalidad.

Validación hojas de cálculo para principiantes
En este blog, podrás encontrar nociones básicas sobre la validación de hojas de cálculo.

Fabricación continua en la industria farmacéutica: Mejora de la producción de medicamentos
La fabricación continua en la industria farmacéutica mejora la eficacia y la calidad del producto. Conoce la aplicación de la fabricación continua, las estrategias de control y las directrices ICH Q13.

Generalidades de la validación de sistemas computarizados
En este blog, nos comprometemos a proporcionarte respuestas detalladas y explicaciones exhaustivas sobre las generalidades de la validación de sistemas computarizados. Además, abordaremos los requisitos necesarios para la validación de sistemas computarizados.

Validación de un ERP: Consejos prácticos
Este articulo proporciona orientación sobre la validación de un ERP (Enterprise Resource Planning) en el giro farmacéutico. Se discuten consejos prácticos, como la identificación de módulos con impacto en la calidad del producto, la integridad del paciente y la integridad de datos, así como la importancia de solicitar PNO’s o instructivos de los módulos con impacto.

Revisión periódica en un sistema computarizado validado: ¿Cuál es su finalidad?
La Revisión Periódica es un proceso de evaluación y mantenimiento que permite garantizar el funcionamiento adecuado y seguro de diferentes sistemas y servicios, identificando y corrigiendo problemas antes de que se conviertan en incidentes graves.

¿Qué es Mapeo Térmico?
Mapeo Térmico: ¿Qué es? Es un proceso mediante el cual se recolectan o se registran datos de temperatura y/o humedad relativa de un espacio determinado,

Calificación de equipos en instalaciones de producción farmacéuticas
En la industria farmacéutica se debe garantizar los procesos de producción y una tarea que hace parte de estos reglamentos es la calificación de equipos,

GAMP 5 Segunda Edición: ¿Qué hay de nuevo?
Descubre las últimas innovaciones en validación de sistemas informáticos con la segunda edición del GAMP 5. Como expertos en digitalización y validación, en este blog te contamos todas las novedades más destacadas que ofrece esta actualización. Optimiza tus procesos, garantiza la calidad y cumple con los estándares más exigentes de la industria de ciencias de la vida.

Elementos esenciales para el monitoreo de temperatura en un sistema
En sectores industriales regulados, hay una creciente demanda para registrar y supervisar en tiempo real las condiciones ambientales (como temperatura, humedad y presión). Esto garantiza

Tres aspectos importantes a considerar antes de validar sistemas computarizados
La mayoría de las empresas parecen no estar preparadas para afrontar con éxito una auditoría regulatoria que les permita obtener la certificación en BPx (buenas

Revisión Anual de la Calidad del Producto en la Industria Farmacéutica: Importancia, ventajas y retos
La Revisión Anual del Producto (RAP) es el análisis histórico de la calidad de un producto, que toma como base todos los documentos normativos en uso en el ámbito farmacéutico (análisis de laboratorio, registros de producción, registros de incidentes, desviaciones, reclamaciones o quejas, devoluciones, etc.), los criterios reconocidos internacionalmente, así como las directrices internas de cada empresa.

La relevancia de la validación que trasciende el cumplimiento de las normas
¿Cuál es la importancia de la validación que va más allá de simplemente cumplir con las regulaciones? Si bien estamos conscientes de la necesidad de

Validación efectiva de hojas de cálculo: consejos clave
¿Cuál es el propósito de la validación de una Hoja de Cálculo? La validación tiene como meta principal la generación de una evidencia documentada que

¿Cuál es la importancia de respaldar sistemas no conectados a la red?
Backup: ¿Por qué se deben realizar? Las empresas que operan en sectores regulados, como el farmacéutico, el cannabis, las clínicas y otros, a menudo tienen

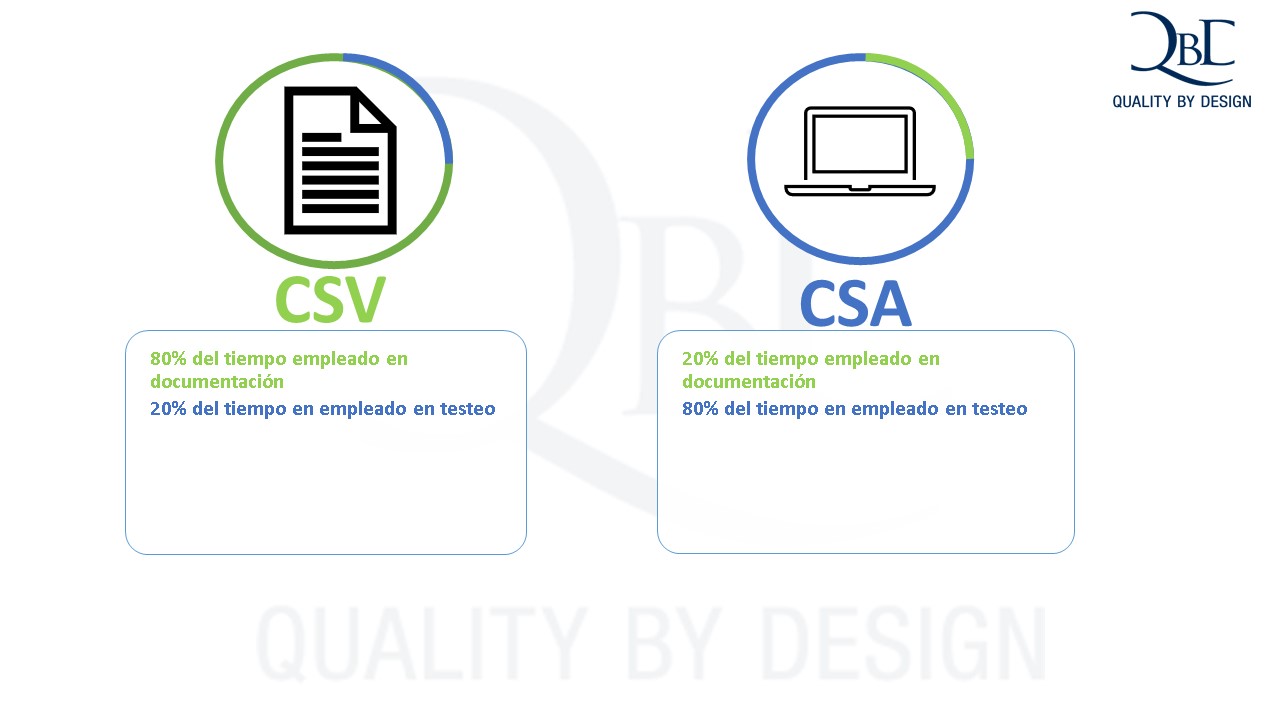
¿Qué es la Garantía de Sistemas Informáticos (CSA) y para qué sirve?
La Garantía de Sistemas Informáticos (CSA) consta en aplicar el pensamiento crítico en el proceso de validación para aplicar el nivel adecuado de pruebas a las actividades de mayor riesgo, con una disminución considerable del tiempo dedicado a la documentación, reduciendo así el esfuerzo de validación y centrando los esfuerzos en mejorar la calidad y el grado de cumplimiento de nuestros procesos empresariales.

¿Cuáles son los componentes clave de un Procedimiento de Operación (POS/SOP)?
Información en un procedimiento de operación (POS /SOP) En este artículo, proporcionaremos pautas sobre la información básica que debe incluir tu procedimiento de operación para

Evaluación de impacto y análisis de riesgos en el proceso de validación
Consideraciones clave para evaluar el impacto de sistemas computarizados antes de validarlos Es esencial considerar varios puntos antes de iniciar la validación de sistemas computarizados

¿Qué se debe tener en cuenta para realizar un mapeo térmico?
En este apartado, abordamos algunas de las preguntas que surgieron durante nuestro webinar online y gratuito sobre Mapeo térmico: ¿Qué se debe tener en cuenta

Validación sin papel: Eficiencia cimentada en la tecnología
La validación sin papel llega al mundo de las ciencias de la vida, facilitando y otorgando nuevas herramientas que apoyarán la gestión documental (en todo su ciclo de vida), integridad de datos, automatización y eficiencia a través de la tecnología.

Clasificación de los sistemas computarizados
Explora la clasificación de sistemas informatizados y sus tipos basados en funcionalidad y diseño

Las etapas de la validación de procesos
El ciclo de vida de la validación de procesos es esencial para garantizar la calidad y la conformidad en la industria. Desde la planificación hasta la ejecución y el monitoreo, cada etapa juega un papel crucial en asegurar la eficiencia y la seguridad de los procesos de fabricación.

Hallazgos frecuentes durante auditorias
En el contexto de la auditoría de validación de sistemas computarizados, se revela la presencia constante de hallazgos recurrentes. En esta ocasión, Johana Sandoval, Gerente

Hojas de cálculo | Preguntas y respuestas
En este apartado, abordamos algunas de las dudas que surgieron durante nuestro pasado webinar online y gratuito sobre Validación de hojas de cálculo dictado por

Generalidades de la validación de procesos | Parte 3
En la tercera parte de nuestra sobre Validación de procesos, te brindamos un completo análisis de la metodología de validación, criterios utilizados, conclusiones clave y

Generalidades de la validación de procesos | Parte 2
En nuestra segunda parte de la cápsula de validación de procesos, te presentamos información sobre la estructura del protocolo de validación, los pre requisitos necesarios,

Generalidades de la validación de procesos | Parte 1
En nuestro primer artículo de la capsula sobre las generalidades de la validación de procesos, exploraremos un poco sobre las BPM y su importancia en

Normas Internacionales para la Verificación de la Validación de Hojas de Cálculo
¿Alguna vez te has preguntado en qué se basan los auditores para verificar la validación de hojas de cálculo? En este apartado, exploraremos las Normas

Introducción al mapeo térmico | 2°Parte
En la segunda parte de nuestra cápsula introductoria al Mapeo Térmico, exploraremos temas como la Etapa I, que abarca la elaboración de un protocolo y

Introducción al mapeo térmico | 1°Parte
En nuestra cápsula introductoria al mapeo térmico, parte 1, encontrarás información sobre la definición del tema, su alcance, las normativas asociadas, los objetivos y requisitos,

La importancia de un software de gestión documental
En este blog, te contaremos todo lo que necesitas saber sobre el software de gestión documental, como debe llevarse la documentación según el manual de buenas prácticas de manufactura y cómo puede beneficiar a tu empresa.

Principales Impactos en la integridad de datos
El artículo examina los principales impactos que pueden comprometer la integridad de los datos en sistemas computarizados. Se identifican cinco tipos de impactos y se enfatiza la necesidad de evaluarlos en los análisis de riesgos. Además, se explica cómo estos impactos pueden surgir y se resalta la importancia de preservar la integridad de los datos mediante atributos y buenas prácticas.

Puntos clave en el mapeo de zonas reguladas
El mapeo de áreas controladas tiene puntos clave y esenciales que debes conocer. Nosotros te los contamos aquí.

Aspectos esenciales para evaluar la calificación de personal
Descubre los 8 puntos clave para verificar la calificación de personal y construir un equipo talentoso y eficiente en nuestro blog.

¿Qué debemos verificar en el IQ según GAMP 5?
En este artículo siguiendo la GAMP 5, veremos la Calificación de instalación (IQ), y te daremos una lista de pruebas genéricas que te permitirá no olvidar ninguna prueba importante.

¿Cuáles sistemas computarizados se deben validar?
¿Estás seguro de saber qué sistemas computarizados necesitas validar?

Validación de sistemas computarizados
¿Estás considerando validar tus sistemas computarizados? Antes de seguir adelante, es importante que conozcas algunos detalles clave que pueden ahorrarte tiempo, dinero y preocupaciones.

Validación de Limpieza
Es crucial entender lo que significa validar la limpieza, al igual que como debe hacerse, que áreas o equipos requieren de validación de limpieza y cuál es la manera correcta de documentarlo.

Plan Maestro de Validación
Te explicamos que debe tener el Plan Maestro de Validación de Sistemas computarizados y la importancia del mismo para cumplir la regulación.

Mantenimiento de Equipos
Este Blog tiene como objetivo, comprender la importancia de un buen mantenimiento de un equipo en su ciclo de vida útil y consejos para ayudar a mantener sus condiciones de uso.

Mapeos térmicos y validación de cadena de frío
¿Qué es? El mapeo térmico es el proceso por el cual adjuntas la evidencia clara y suficiente sobre los valores de temperatura y humedad relativa

Validación de Métodos Analíticos
¿Sabes que es validación de métodos analíticos? ¿Por qué validar métodos analíticos? ¿Para qué validar los métodos analíticos? ¿Cuándo validar los métodos analíticos? En
Plan Maestro de Validación
El objetivo del Plan Maestro de Validación (PMV) específica y coordina todas las actividades de cualificación / validación con el propósito de asegurar que la
Aquí encontrará artículos y noticias interesantes relacionados con su sector.