Gracias por apuntarte al webinar
Gracias por registrarse en nuestro seminario web. A medida que se acerque la fecha del seminario web, nos aseguraremos de enviarle más información. ¿Sediento de conocimiento? Mientras tanto, asegúrese de explorar nuestros artículos sobre Life Sciences a continuación.

Por qué los desafíos de la GC en los ATMP son diferentes y lo que necesita saber
En esta entrada del blog, ofrecemos más información sobre los retos a los que se enfrenta un QP cuando trata con ATMPs. Hablamos de la esterilidad, la manipulación fuera de especificación, la liberación de lotes y las pruebas de importación de la UE.

Fábricas inteligentes: Cómo los gemelos digitales pueden mejorar fuertemente sus procesos de fabricación de ATMP
En las fábricas inteligentes que llegaron con la Industria 4.0, los gemelos digitales de los procesos de fabricación son clave para mejorar la solidez de los procesos, los plazos de desarrollo y, en última instancia, reducir los costes. En este blog, Evan Claes y Tommy Heck, de nuestro socio Antleron, explican cómo funcionan los gemelos digitales y por qué son tan vitales, sobre todo para la fabricación de ATMP.

10 cosas que debe saber antes de validar los sistemas informáticos
¿No sabe por dónde empezar a validar sus sistemas informáticos? Siga estos 10 pasos como guía.

De la idea a la vigilancia posterior a la comercialización: las fases del ciclo de vida de los productos sanitarios
El lanzamiento de un producto sanitario requiere mucha preparación. Como estos dispositivos están fuertemente regulados, una empresa tiene que cumplir muchos requisitos en diferentes fases del proceso de desarrollo y fabricación. ¿Qué fases hay que tener en cuenta y cuáles son sus características? Este blog profundiza en el ciclo de vida de un producto sanitario y en los requisitos que deben cumplirse en esas fases.

Ensayos clínicos para los ATMP: ¿qué retos hay que superar?
Los ATMP son, por naturaleza, terapias muy complejas e innovadoras. Y los ensayos clínicos bien diseñados son la clave para producir medicamentos de terapia avanzada eficaces y seguros, lo que en última instancia aumenta la salud de los pacientes y acelera la autorización de comercialización. En esta entrada de blog, Marie-Paule Gyselen de TRIUM Clinical Consulting (parte del Grupo QbD) le guía a través de los retos más importantes de los ensayos clínicos específicos de ATMP.

Cómo la QbD está invirtiendo en la nueva forma híbrida de trabajar
En QbD, vamos a hacer un esfuerzo adicional para que el trabajo híbrido beneficie a todos después de COVID-19. ¿Necesita inspiración? Siga nuestro ejemplo.

Por qué la gestión de riesgos de los productos sanitarios es tan compleja como crucial
La gestión de riesgos, la clave de la seguridad de los productos sanitarios, implica mucho más que marcar la casilla del AMFE. Jeroen Verhoeven, uno de nuestros especialistas en la materia, le explica por qué y le guía a través de la norma ISO14971 (aplicación de la gestión de riesgos a los productos sanitarios).

¿Su producto es un dispositivo médico? Bueno, eso depende…
Que su producto sea un producto sanitario depende de los mercados en los que quiera entrar y de su normativa. He aquí un resumen para guiarte.

QbD y TRIUM’s 10Y International Sports Challenge: ¡una mezcla de diversión, ejercicio y espíritu de equipo!
El deporte siempre ha sido una parte esencial del QbD y del ADN de TRIUM. Así que, para celebrar nuestros dos aniversarios de 10 años, hemos ideado un emocionante evento que combina todos estos valores: ¡nuestro 10Y International Sports Challenge! Léalo todo aquí.

ATMPs: traducir la experiencia en un proceso GMP
Los ATMP son un nuevo y prometedor tipo de medicamentos. Aprenda más sobre los retos que supone trasladar la experiencia a un proceso GMP.

5 consecuencias del Brexit en la venta de productos sanitarios en el Reino Unido
El Brexit afecta a los mercados de productos sanitarios de Escocia, Inglaterra, Gales e Irlanda del Norte. Obtenga más información sobre las consecuencias para los fabricantes que comercializan productos sanitarios en el Reino Unido aquí.

SaMD frente a MDSW: ¿cuál es la diferencia entre el software como dispositivo médico y el software para dispositivos médicos?
Los términos SaMD (Software as a Medical Device) y MDSW (Medical Device SoftWare) suelen utilizarse indistintamente en los entornos médicos, pero no lo son. Conozca aquí la diferencia de significado y alcance normativo.

Desentrañar la inteligencia artificial en los dispositivos médicos: ¿qué sabemos hasta ahora?
La Inteligencia Artificial es la palabra informática en los dispositivos médicos hoy en día. Más información sobre la IA y sus implicaciones normativas para los fabricantes.

La Academia de QbD da la bienvenida a 15 jóvenes graduados para impulsar sus carreras en las ciencias de la vida
La Academia QbD es un programa para jóvenes graduados que combina trabajo, aprendizaje y formación intensiva. El mes pasado, dimos la bienvenida a 15 jóvenes graduados durante nuestra Semana de la Academia de QbD. Lea todo sobre ello aquí.
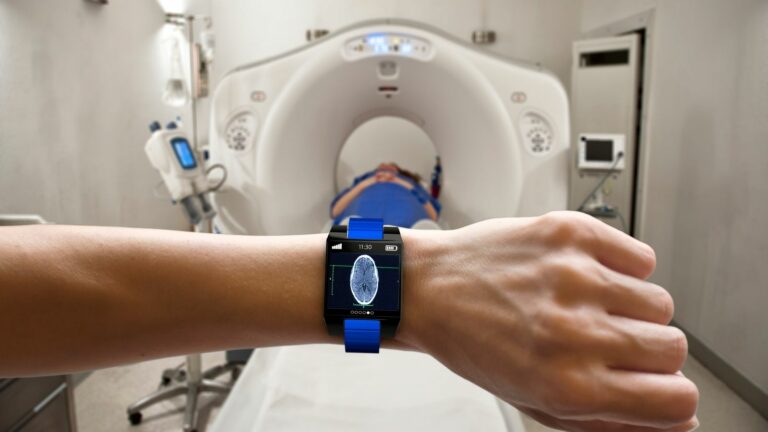
Tendencias de la industria de dispositivos médicos: sobre wearables, IA, pruebas POC, IoT y más
¿Tiene curiosidad por conocer las últimas tendencias del sector de los dispositivos médicos? Obtenga más información sobre los wearables, la IA, las pruebas POC, el IoT y mucho más en esta publicación del blog.

Impacto de la MDR en la MDSW: ¿qué ha cambiado con respecto a la MDD?
La introducción del MDR afecta al software médico con marcado CE (MDSW). ¿Tiene curiosidad por conocer el alcance de este impacto en su software? Lea más abajo.

Clasificación IVDR de los productos sanitarios de diagnóstico in vitro: breve guía para los fabricantes
Obtenga más información sobre el nuevo enfoque basado en el riesgo para la clasificación de dispositivos de diagnóstico in vitro en virtud del IVDR 2017/746, que sustituye a las directivas obsoletas.

Productos combinados de productos sanitarios: ¿qué normas debe aplicar antes de comercializarlos en la UE?
Siga estos pasos antes de lanzar productos combinados de productos sanitarios en la UE, incluida la aplicación del artículo 117 del MDR y la Directiva de la EMA.
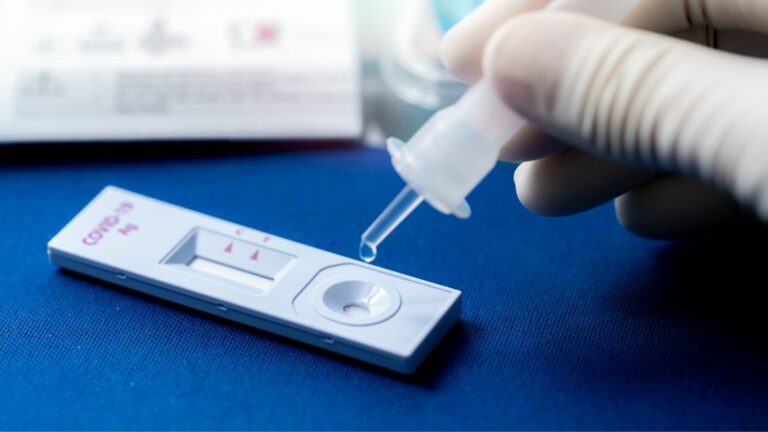
De IVDD a IVDR: evite estos escollos para conseguir el marcado CE a tiempo
En la UE, el IVDR sustituirá al IVDD. El plazo de cumplimiento se acerca, así que actúe ahora para obtener el marcado CE de su dispositivo médico IVD a tiempo.
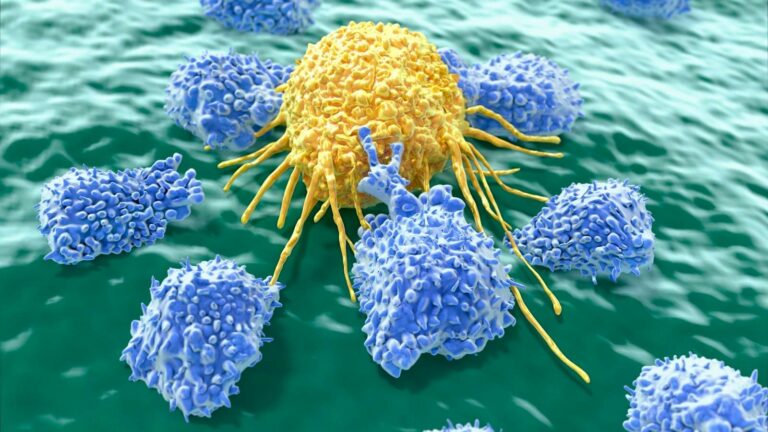
Por qué las células NK son un gran avance en el campo de los ATMP
Las células NK, como parte de nuestro sistema inmunitario innato, son muy eficaces para eliminar diferentes tipos de células, incluidas las tumorales. Debido a estas propiedades, resultan muy interesantes como ATMP para la inmunoterapia.
¿Siente curiosidad por el potencial de las células NK y la inmunoterapia basada en ellas? Conozca aquí todo sobre ellos, incluidas las ventajas y los retos.
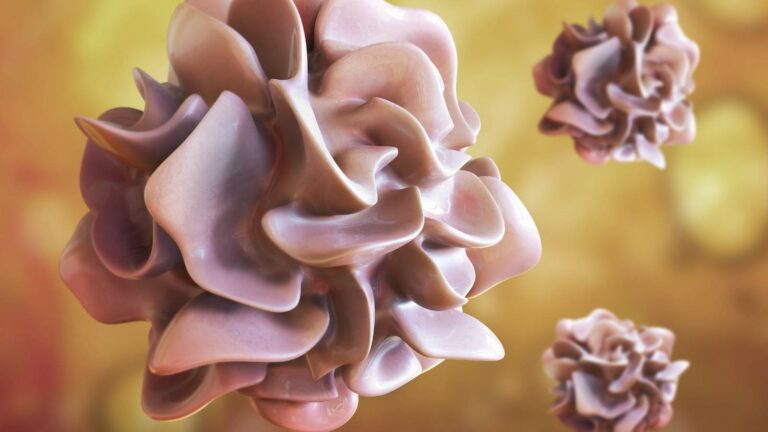
Células dendríticas: centinelas eficaces para las inmunoterapias
Las células dendríticas desempeñan un papel importante en las inmunoterapias basadas en DC desarrolladas recientemente para el tratamiento del cáncer, las enfermedades autoinmunes y la prevención del rechazo de injertos. Lea todo sobre las células DC y su potencial en este artículo.

QbD y TRIUM reciben el certificado Baanbrekende Werkgever ’22
El 15 de noviembre de 2021, QbD y TRIUM recibieron el certificado Baanbrekende Werkgever ’22 por ser empleadores belgas pioneros que se esfuerzan por poner a las personas en el centro de sus políticas de trabajo híbrido y movilidad.

10 preguntas para el «chico del 10º aniversario» Jeroen Verhoeven
Si sabes que QbD se fundó hace 10 años, no te sorprenderá que el décimo aniversario de un empleado sea un acontecimiento EXTRA grande para nosotros. Después del fundador de QbD, Bart (obviamente), Jeroen Verhoeven es el primer empleado que alcanza ese hito.
Para dar a esta noticia la atención que merece, hemos lanzado 10 preguntas a Jeroen, una por cada año que lleva con nosotros.
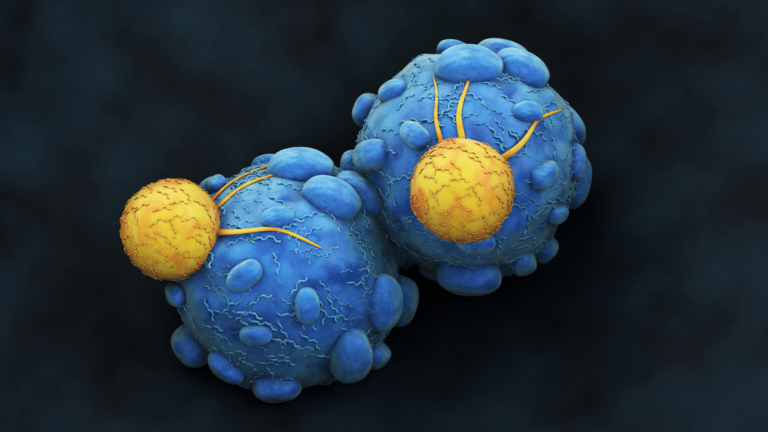
La terapia celular como un ATMP: introducción, definición y subtipos
La terapia celular incluye varios ATMP para luchar contra los tumores o restaurar el estado fisiológico de los tejidos dañados. Explórelos aquí.

Un día en la vida de un especialista en QbD MD
Los dispositivos médicos son una de las principales áreas de experiencia de QbD. Le apoyamos desde el concepto hasta el lanzamiento en todo el ciclo de vida. ¿Se pregunta cómo es un día en la vida de un especialista en QbD MD? Echemos un vistazo entre bastidores.

Retos del control de calidad en sistemas cerrados: aplicación de la IA como control en el proceso
La toma de muestras, la realización de pruebas y la conservación de su medicamento en sistemas cerrados suelen plantear difíciles retos de control de calidad. Como parte de la solución, se pueden utilizar varios controles en proceso basados en la IA. ¡Descúbralos aquí!

El papel clave de Asuntos Regulatorios en la industria farmacéutica: desde el desarrollo del medicamento hasta su comercialización
Los asuntos reglamentarios desempeñan un papel fundamental en la industria farmacéutica: desde el desarrollo del medicamento hasta su comercialización. Obtenga más información sobre los papeles y las funciones que los equipos de AR pueden proporcionar en la gestión del ciclo de vida de su producto farmacéutico.

La impresión 3D permite crear dispositivos médicos específicos para el paciente para mejorar la calidad de la asistencia
La impresión 3D ofrece una flexibilidad y una personalización inigualables en los dispositivos médicos, como ilustra el caso del trasplante de cara y mano de Joe DiMeo. ¿Tienes curiosidad? No deje de leer.

10 preguntas para la «chica del 10º aniversario» Katrien Janssens
¡10 años! Ese es el tiempo que Katrien Janssens lleva trabajando en QbD. Enhorabuena. ¿Tiene curiosidad por saber cómo ha vivido Katrien la última década en QbD? Durante una breve entrevista, le hicimos 10 preguntas rápidas: ¡una por cada año que ha trabajado con nosotros!

¿Qué es EUDAMED y qué nuevos requisitos deben tener en cuenta las empresas de productos sanitarios?
La nueva normativa sobre productos sanitarios y la correspondiente aplicación de EUDAMED pretenden dar al público en general acceso a la información pertinente sobre los productos sanitarios, garantizando una mayor transparencia. Sin embargo, EUDAMED también aporta nuevos requisitos para los participantes en el mercado a lo largo del ciclo de vida de los productos sanitarios. Lea más sobre ellos aquí.

10Y Dominiek Rossillion en QbD: de ingeniero de calidad a director de desarrollo empresarial
Dominiek Rossillion lleva 10 años trabajando en QbD, ¡y contando! Nuestra más sincera enhorabuena. ¿Tienes curiosidad por conocer la carrera de Dominiek y sus opiniones? Entonces no deje de leer esta entrevista.
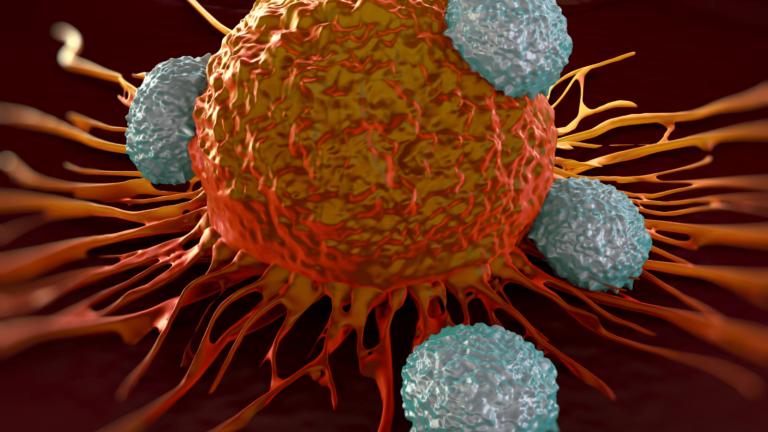
Terapia con células CAR-T: destacando los principales componentes, el proceso de fabricación y las perspectivas
La terapia celular CAR-T utiliza células T modificadas genéticamente para destruir las células tumorales. Conozca los principales componentes, el proceso de fabricación y las perspectivas de esta prometedora inmunoterapia.

EDQM y el CEP del futuro
Se considera que un certificado de adecuación a las monografías de la Farmacopea Europea (CEP) emitido por la EDQM sustituye a los apartados correspondientes de la solicitud de autorización de comercialización que demuestran la calidad de las sustancias de uso farmacéutico. La inclusión de un PEC en un AMS simplifica el proceso de revisión para las autoridades y los procedimientos de presentación para la industria. Sin embargo, con los próximos cambios en la legislación farmacéutica de la UE, el procedimiento CEP puede estar en peligro. En esta entrada del blog, exponemos los posibles cambios en un futuro próximo.

Evaluación clínica de los productos sanitarios en el marco del MDR: guía breve
La evaluación clínica de los productos sanitarios es fundamental para obtener y mantener la autorización de comercialización en la UE. Más información sobre la evaluación clínica aquí.

10Y Steven Vinkx en QbD: de ingeniero de proyectos a jefe de la PMO
Steven Vinkx lleva 10 años trabajando para la QbD, y contando. Enhorabuena. ¿Tiene curiosidad por conocer su carrera y sus ideas? Entonces no deje de leer esta entrevista.

Plan de evaluación clínica (PEC): hoja de ruta de la estrategia de evaluación clínica
El Plan de Evaluación Clínica, o CEP, es un punto de partida crucial y una guía para la evaluación clínica de su producto sanitario. Obtenga más información sobre este documento clave y sus requisitos.

Informe de evaluación clínica (CER): imprescindible para todas las clasificaciones de productos sanitarios
Para documentar la evaluación clínica de su dispositivo y sus resultados, hay que elaborar un informe de evaluación clínica o CER. Obtenga más información sobre este documento clave, su contenido, las lagunas y los obstáculos más comunes.
Nuevo anexo 21 de las BPF «Importación de medicamentos»: ¿está usted preparado?
El 21 de agosto de 2022 entrará en vigor el nuevo Anexo 21 de las GMP. Este anexo contiene los requisitos de las prácticas correctas de fabricación para los titulares de MIA cuando importan medicamentos de fuera de la UE/EEE. Obtenga más información aquí.

Conozca a Catarina Cruz, embajadora de QbD y especialista en conformidad de dispositivos
En QbD, valoramos la opinión de nuestros empleados. Por ello, se formó la Junta de Embajadores de QbD para representar la voz de todos los QbD’s, en todo el Grupo QbD y más allá de las fronteras. Catarina Cruz ha sido elegida como una de nuestras embajadoras para 2022. Enhorabuena. Como embajadora, a Catarina le encanta compartir su experiencia de trabajo en QbD. ¿Quieres saber más sobre su trabajo #QbDream? No deje de leer la entrevista a continuación.

Conozca a Marijn Bollema, embajadora de QbD e ingeniera de validación
En el QbD Group, la opinión de nuestros empleados es importante. Por ello, formamos una Junta de Embajadores para representar la voz de todos los QbD’ers, dentro y fuera del grupo. Marijn Bollema ha sido elegida como una de nuestras embajadoras para 2022. ¡Felicidades! Como embajador, Marijn quiere mostrar al mundo lo que es ser un verdadero QbD. ¿Quieres saber más sobre su trabajo #QbDream? No deje de leer la entrevista a continuación.

Conozca al embajador de QbD y al director del proyecto de Farmacología Clínica y Farmacometría, Thomas Van Looy
En el QbD Group queremos tener en cuenta la opinión de nuestros empleados. Por lo tanto, nuestra Junta de Embajadores fue elegida para representar la voz de todos los QbD’ers, dentro y fuera del grupo. Thomas Van Looy ha sido elegido como uno de nuestros embajadores para 2022. ¡Felicidades, Thomas! Como embajador, le encanta compartir sus experiencias con el Grupo QbD. ¿Quieres saber más sobre el trabajo #QbDream de Thomas? Entonces no se pierda la entrevista que le presentamos a continuación.

Gases comprimidos en la fabricación de productos farmacéuticos: mejores prácticas de control microbiano
El aire comprimido y otros gases de proceso se utilizan en muchos pasos diferentes durante la fabricación de productos farmacéuticos. Algunos ejemplos son el uso de aire comprimido en contacto directo con los productos para limpiarlos, airearlos o moverlos a través de los procesos o el uso de gases de proceso en bombas de fluidos que llevan los productos a través de los procesos de producción y llenado. Los gases comprimidos, como el nitrógeno o el argón, también pueden utilizarse para cubrir o rociar un producto. Los riesgos asociados a la utilización de estos gases dependen de la cantidad y el tipo de contacto con el producto y, sobre la base de esta evaluación de riesgos, debe establecerse un plan de seguimiento adecuado.

6 mitos comunes sobre la consultoría en ciencias de la vida
¿Está pensando en una apasionante carrera como consultor en ciencias de la vida, pero aún tiene dudas? En este artículo, desmontamos 6 mitos sobre la asesoría para ayudarte a decidir.

Persona responsable del cumplimiento de la normativa o «PRRC»: significado, requisitos y responsabilidades
El Reglamento de Dispositivos Médicos (MDR) (UE) 2017/745 y el Reglamento de Dispositivos In Vitro (IVDR) (UE) 2017/746 introdujeron una nueva función obligatoria en el artículo 15: la persona responsable del cumplimiento normativo o «PRRC». ¿Se pregunta qué significa el papel de PRRC y dónde puede encontrar a la persona adecuada? Entonces, ¡siga leyendo!
La publicidad de los medicamentos en Bélgica: un breve resumen de la normativa
En Bélgica, la publicidad de los medicamentos está sujeta a la legislación para garantizar el uso racional de los mismos. Cada empresa debe designar a un responsable de la información y la publicidad, que comprueba la conformidad de la publicidad.
La vía reglamentaria para su producto sanitario a medida
¿Es usted un fabricante de productos sanitarios a medida y necesita orientación normativa? Este artículo resume las principales preocupaciones que hay que tener en cuenta.

Por qué las autoinspecciones o auditorías internas son esenciales para su SGC
Las autoinspecciones o auditorías internas son una parte esencial de su SGC. Además de determinar si su SGC cumple las directrices y normas, puede beneficiarse de ellas de varias maneras. Permiten conocer mejor los departamentos, explicar a la gente por qué son necesarios determinados procesos de calidad, recopilar información útil para mejorar el SGC y disponer de una herramienta para comprobar su preparación para las auditorías externas.

Categorías GAMP para sistemas informáticos: ¿qué son y para qué sirven?
Las categorías GAMP son muy importantes para decidir la estrategia de validación de su sistema informático. Conozca más sobre todas las categorías aquí.

Validación de Hojas de Cálculo: ¿qué debo saber?
Este blog tiene como objetivo exponer en un resumen la información básica que cualquier persona que se esté introduciendo en el universo de la validación
Sistemas Informáticos: ¿es la nueva validación una garantía?
El concepto de Validación de Sistemas Informáticos hasta ahora nos ha servido bien y nos ha proporcionado la base de donde estamos hoy. Pero en
Del CCKL a la ISO 15189: lo que debe saber
Los laboratorios clínicos y patológicos de los Países Bajos están experimentando grandes cambios. Un número creciente de ellas solicita la acreditación del «Raad voor Accreditatie»

Eudralex Vol 4: Nuevo anexo 15: Cualificación (PARTE 2)
Validación de procesos La sección de validación de procesos ha doblado su tamaño de 2 a 4 páginas, con secciones adicionales sobre la verificación
EudraLex Vol 4: Nuevo anexo 15: Cualificación
A partir del 1 de octubre de 2015, la revisión del anexo 15 de EudraLex Vol 4 entrará en funcionamiento, cualificación y validación. El anexo
Productos combinados – deel 3
La última parte del borrador de las directrices de la FDA para los productos combinados, con una descripción detallada de los dos últimos artículos. Ficha
Productos combinados – deel 2
Para la interpretación de los dos primeros artículos de este mes, consulte el artículo 3: Consideraciones generales para el cumplimiento de las CGMP: A. Demostrar
Un San Valentín de calidad
Hoy es San Valentín, por lo que quizás le hayan regalado un perfume u otro regalo de cosmética, o bien haya sorprendido a su pareja
Novedades de EMA (3)
A principios de año, EMA publicó una revisión de la “Guideline on the acceptability of names for human medicinal products”. En lo sucesivo, ante una
Novedades de EMA (2)
A pesar de no ser ninguna razón de preocupación para los usuarios y los fabricantes, EMA, la European Medicines Agency, ha iniciado el análisis de
¿Qué es ANDA?
ANDA son las siglas para Abbreviated New Drug Application. Un ANDA es un archivo que se presenta ante la FDA para una variante genérica sobre
Novedades de EMA (1)
Visto que EMA lo ha incorporado en la lista de preguntas y respuestas, será una pregunta procedente de la industria: “¿Se considera aceptable añadir un
Nuevo en la FDA (3)
Nueva guía para la validación de métodos analíticos La FDA ha publicado una nueva Guía de Validación de Métodos Analíticos. Esto significa que el anterior,
Novedades de la FDA (2)
Preparación para la FDA Con motivo de una inspección por la temida FDA, el término de FDA readiness (preparación para la FDA), ha aparecido en
Nuevo en la FDA (1)
Más inspecciones en todo el mundo Una noticia muy interesante, ya que la FDA ha aprobado un nuevo presupuesto más amplio que el anterior. Por
Aquí encontrará artículos y noticias interesantes relacionados con su sector.