Los productos sanitarios de diagnóstico in vitro(IVD )(Fabricantes | Mercado Interior, Industria, Emprendimiento y PYME (europa.eu)) han ganado mucha atención en las últimas décadas.
La crisis de la corona nos ha enseñado que el diagnóstico rápido y correcto, que requiere dispositivos médicos IVD, es una parte esencial del sistema sanitario mundial. Desde las autopruebas relativamente sencillas en el embarazo hasta los complejos diagnósticos de laboratorio de última generación, los DIV abarcan una amplia gama de equipos y pruebas.
Con esta tendencia al alza en el mercado del DIV, se introdujeron nuevas y estrictas regulaciones para garantizar la alta calidad, el fuerte rendimiento y la seguridad para todos.
Antes de 2017, la Directiva IVD (IVDD ) establecía los requisitos reglamentarios para el marcado CE. Esta directiva se amplió al Reglamento sobre DIV (IVDR), que introdujo una regulación armonizada en Europa con normas más estrictas para comercializar los DIV. El IVDR se publicó en mayo de 2017 y entrará plenamente en vigor en mayo de 2022.
Este blog le guiará a través de los principales cambios y escollos a los que se enfrentarán los fabricantes de DIVs antes de la plena aplicación del IVDR.
Cómo introducir un DIV en el mercado según el nuevo IVDR (Reglamento (UE) 2017/746)
El Reglamento (UE) 2017/746 (L_2017117ES.01017601.xml (europa.eu)) de la Unión Europea (IVDR) es la normativa específica para los productos sanitarios IVD desde 2017 y sustituirá totalmente a la Directiva 98/79/CE que la deroga en 2022. No se ha producido ningún cambio en el IVDR con respecto al IVDD, pero se han añadido nuevos requisitos que incluyen:
- cambios en la clasificación de los dispositivos
- una supervisión más estricta de los fabricantes por parte de los organismos notificados
- requisitos más estrictos para las pruebas clínicas y la evaluación de la conformidad
- especificaciones comunes
A diferencia de la DIV, el DIV no necesita ser transpuesto a la legislación nacional, lo que reduce los riesgos de discrepancias de interpretación en el mercado de la UE.
Una adición importante del IVDR fue la introducción de 4 clases de riesgo de dispositivos médicos IVD, de bajo a alto riesgo: A, B, C y D. Puede encontrar más información sobre esta nueva clasificación de riesgo aquí.
Los DIVs en los que se aplican condiciones generales de riesgo vital pueden ser contabilizados como la clase D de mayor riesgo y necesitan una revisión más extensa para conseguir su certificación europea, que se explicará más adelante.
La aplicación del DIVR no es sencilla, y las especificaciones pueden ser más difíciles de interpretar para el personal inexperto. Se requieren diferentes procedimientos de evaluación en función de la clase de riesgo del producto y, en el caso de los medicamentos, se debe consultar a las autoridades competentes.
IVDR: 3 escollos comunes en el camino
1. Mayor participación de los organismos notificados
Con la DIV, el 90% de los productos sanitarios de DIV podrían autocertificarse. Con el nuevo IVDR, el 85% de los productos necesitarán un organismo notificado para obtener el marcado CE. Sólo los productos no estériles de clase A pueden seguir siendo autocertificados. Un organismo notificado es una organización designada por una autoridad competente de un Estado miembro de la UE que realiza evaluaciones de conformidad para verificar que un producto puede ser comercializado.
Todos los productos permitidos anteriormente en el mercado tendrán que ser reclasificados y registrados de nuevo, lo que introducirá una enorme sobrecarga normativa. Se necesitan aproximadamente 12 meses para completar un expediente en el marco de la DIV y conseguir el marcado CE para los DIV de alto riesgo. El IVDR aumenta la carga de trabajo antes de la autorización de comercialización, lo que aumenta aún más este tiempo de aplicación.
Sólo un número limitado de organismos notificados cumplen los requisitos más estrictos del IVDR y, por tanto, ya están disponibles. Con el fin del periodo de transición a la vista, sólo será más difícil conseguir el marcado CE a tiempo. Contar con expertos con los conocimientos y conexiones necesarios será crucial para guiarle en este proceso.
2. Los productos sanitarios innovadores y de alto riesgo de IVD requieren una revisión por parte de un panel de expertos
Existen requisitos aún más estrictos para los dispositivos de mayor riesgo. Estos dispositivos de clase D se utilizan para detectar agentes que contienen un alto riesgo individual o público. Se utilizan para la detección de agentes transmisibles en la sangre, las células o los tejidos o para la detección de agentes transmisibles que causan una enfermedad potencialmente mortal como el ébola o la malaria.
El grupo de coordinación de productos sanitarios (MDCG ) es responsable de la aplicación armonizada del IVDR. Han introducido una recomendación obligatoria para los productos de la clase de mayor riesgo (D), en la que el organismo notificado debe comprobar con un panel de expertos individuales el rendimiento declarado por el fabricante. Las pruebas deben realizarse en laboratorios de referencia de la UE.
No todos los dispositivos de alto riesgo necesitan pasar por este procedimiento, sólo cuando el dispositivo es el primero de su tipo. Esto debe interpretarse de la siguiente manera: aún no se han publicado especificaciones comunes en el Diario Oficial de la UE y aún no se ha concedido ningún certificado en virtud de la DIV o el DIVR para dicho producto. Los criterios utilizados para determinar si un dispositivo de DIV es el primero de su clase se basan en dos principios. O bien la finalidad prevista o la tecnología de análisis es nueva en el mercado.
3. El periodo de transición: el tiempo se acaba
Actualmente estamos en pleno periodo de transición de la DIV a la DIVR para aplicar estas estrictas normas. El calendario completo de la transición se detalla en la siguiente figura.
Los fabricantes tendrán que cumplir plenamente el IVDR el 26 de mayo de 2022. Se recomienda encarecidamente iniciar la transición lo antes posible debido al elevado número de dispositivos que se prevé que haya en el mercado y al previsible cuello de botella en las revisiones por parte del limitado número de organismos notificados. La presión sobre estos organismos notificados no hará más que aumentar a medida que se acerque la fecha límite.
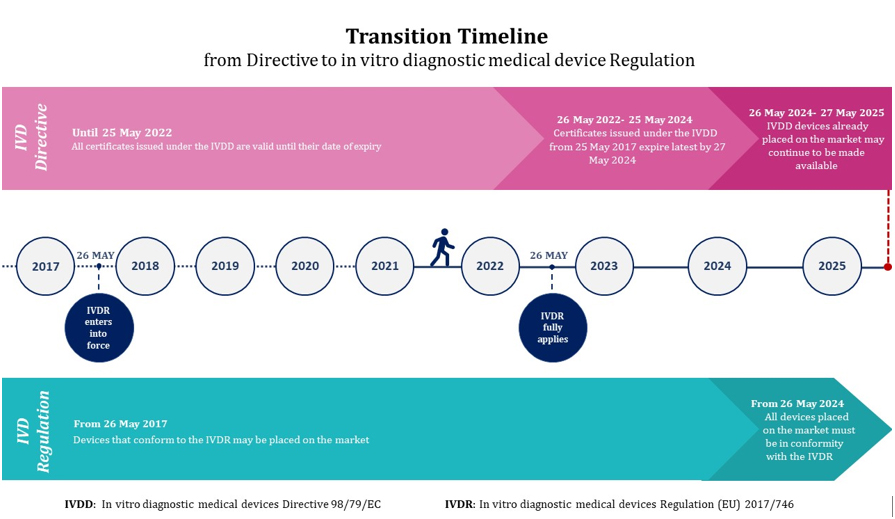
Figura 1 – Cronología de la transición del DIV al DIVR
ADENDA 14 DE OCTUBRE
El 14 de octubre de 2021, la Comisión Europea propuso un puesta en marcha gradual del nuevo Reglamento sobre productos sanitarios para diagnóstico in vitro para evitar la interrupción del suministro de estos productos sanitarios esenciales.
La propuesta no supone un cambio sustancial de los requisitos del reglamento sobre productos sanitarios para diagnóstico in vitro (DIV), sino que sólo modifica las disposiciones transitorias para permitir la implantación gradual del reglamento.
La duración de los periodos de transición propuestos depende del tipo de producto: los productos de mayor riesgo, como las pruebas del VIH o la hepatitis (Clase D) y determinadas pruebas de la gripe (Clase C), tendrán un período de transición hasta mayo de 2025 y 2026, mientras que los productos de menor riesgo, como los productos estériles de clase B y A, tendrán un período de transición hasta mayo de 2027.
El IVDR está llamando a la puerta, ¡obtenga ya el marcado CE!
El nuevo IVDR no sólo introduce un nuevo sistema de clasificación de productos, sino que también establece normas más estrictas para la calidad de estos productos sanitarios IVD.
Especialmente en el caso de los productos sanitarios IVD más innovadores y de mayor riesgo, será necesario un esfuerzo adicional para llevar su producto al mercado. A medida que se acerca la fecha límite, los consultores, los profesionales internos y los organismos notificados estarán más ocupados, así que actúe ahora para estar preparado a tiempo.
¿Todavía tiene muchas preguntas sobre el marcado CE, el DIV y el DIVR, o le desaniman estos escollos? ¿Está comercializando un nuevo DIV y no sabe por dónde empezar? La ayuda de QbD está a sólo un correo electrónico o una llamada telefónica de distancia. Nuestros expertos internos estarán encantados de guiarle por el camino.