
CRO de Dispositivos Médicos
QbD Clinical es un CRO de servicio completo dedicado a empresas de dispositivos médicos. Desde estudios piloto y de viabilidad hasta ensayos clínicos globales y estudios PMCF, acompañamos a nuestros promotores.
A través de una combinación de experiencia interna y colaboraciones internacionales de confianza, nuestros clientes se benefician de la profunda experiencia de nuestro equipo en cada paso de su investigación clínica. Ayudamos a los patrocinadores a navegar los requisitos del MDR europeo y la FDA, garantizando investigaciones clínicas conformes, eficientes y centradas en el paciente, alineadas con su estrategia de acceso al mercado.
Ya sea que planifiques un estudio europeo o una investigación clínica global, actuamos como tu socio único desde la estrategia hasta la ejecución, facilitando una comunicación más clara, operaciones más fluidas y resultados más rápidos.
Dónde operamos
Cobertura global
Con oficinas en toda Europa y una red de confianza de socios internacionales, apoyamos investigaciones clínicas de dispositivos médicos en todo el mundo, desde el inicio del estudio hasta el cierre.
Cobertura directa del equipo QbD
Bélgica, Polonia, Países Bajos, Luxemburgo, Francia, Reino Unido, Alemania, España, Austria, Suiza
A través de socios y proveedores preferidos
Expansión posible a través de proveedores y socios
¿Cómo podemos ayudarte?
Áreas terapéuticas principales
Apoyamos a fabricantes de Dispositivos Médicos en diversas áreas terapéuticas, ayudándoles a generar evidencia clínica robusta tanto para el cumplimiento del MDR europeo, incluida la transición MDR para dispositivos heredados, como para el acceso al mercado global.
Además de nuestra amplia experiencia en la navegación de las vías regulatorias de la UE, también proporcionamos soporte estratégico y operativo para presentaciones ante la FDA, incluyendo pre-submissions, 510(k) y solicitudes PMA. Mantenemos la supervisión y gestión europea completa de los estudios clínicos para garantizar una ejecución de alta calidad y preparación regulatoria en todas las regiones.
Neurología
Experiencia en dispositivos neurológicos, tecnologías de ictus y soluciones de neuromonitorización.
Ortopedia
Estudios para implantes ortopédicos, dispositivos musculoesqueléticos y tecnologías de rehabilitación.
Offerings
Servicios destacados9

Tu socio CRO único desde la estrategia hasta la ejecución
Guiamos a los patrocinadores de Dispositivos Médicos a través de los requisitos del MDR europeo y la FDA, garantizando investigaciones clínicas conformes, eficientes y centradas en el paciente, alineadas con tu estrategia de acceso al mercado.
Por qué elegirnos
¿Por qué elegir QbD Clinical como tu CRO de Dispositivos Médicos?
Un CRO dedicado, creado para la complejidad y las exigencias regulatorias de la investigación clínica de Dispositivos Médicos.
Enfoque profundo en Dispositivos Médicos
Nos especializamos exclusivamente en Dispositivos Médicos: desde Clase I a Clase III, implantables activos y SaMD. Sin proyectos paralelos de Pharma que distraigan nuestra atención.
Solidez regulatoria
Nuestros expertos internos te ayudan a cumplir con EU MDR, ISO 14155, GCP, GDPR y la normativa local en todos los mercados objetivo.
Ejecución global de ensayos
Con experiencia en la realización de ensayos de Dispositivos Médicos en Europa, Norteamérica y APAC, con redes de centros de confianza en todo el mundo.
Modelo flexible y escalable
Nuestros servicios CRO modulares escalan con tu proyecto: desde estudios iniciales de viabilidad y arranque hasta ensayos pivotales y seguimiento poscomercialización.
Colaboración integrada
Nos integramos sin fisuras con tu equipo interno o tus socios OEM para maximizar la eficiencia y los resultados.
Nuestro equipo
Conoce a nuestros expertos
Realizar ensayos clínicos para Dispositivos Médicos requiere una combinación única de conocimiento regulatorio, experiencia clínica y una profunda comprensión de los requisitos específicos del dispositivo.

Dr. Diane Fairweather
Head of Global Clinical Division
Más de 20 años de liderazgo en investigación clínica.
- Más de 20 años en investigación clínica y desarrollo de Dispositivos Médicos
- Supervisión estratégica de programas clínicos globales
- Profunda experiencia en EU MDR, FDA y marcos regulatorios internacionales

Julie Hendrickx
MD CRO Project Management Lead
Más de 20 años de experiencia en gestión de proyectos clínicos.
- Experiencia internacional en el ámbito Pharma y Dispositivos Médicos
- Más de 8 años como Clinical Project Manager
- Gestión de proyectos desde el inicio del estudio hasta el cierre

Petra De Geest
Business Unit Manager Medical Affairs
12 años de experiencia en el campo de Dispositivos Médicos.
- Evidencia clínica y redacción médica para Dispositivos Médicos (Clase I a Clase III, incluyendo MDSW y MDSW impulsado por IA)
- Gestión de seguridad en investigaciones clínicas de Dispositivos Médicos
- Liderazgo estratégico y consultoría

Sarah Andries
Senior Consultant RA
12 años de experiencia en el campo de Dispositivos Médicos.
- 10 años en Clinical Regulatory
- Presentaciones ante autoridades regulatorias y comités de ética
- MDR y legislación y requisitos nacionales (UE)
- Representante Legal en la UE
Consejo Asesor
Conoce al Consejo Asesor
Nuestro Consejo Asesor Médico reúne a profesionales experimentados en Life Sciences que proporcionan orientación experta sobre estrategia clínica, seguridad del paciente, rigor científico y cumplimiento regulatorio.

Pierfrancesco Agostoni
Cardiólogo intervencionista
- Más de 20 años de experiencia en cardiología invasiva e intervencionista
- Realiza entre 300 y 400 PCI complejas y unas 80 intervenciones TAVI al año
- Experto en intervenciones CTO, acceso radial y técnicas percutáneas avanzadas
- Más de 310 publicaciones indexadas en PubMed y más de 10 capítulos de libros

Gijs Klarenbeek
Médico y experto en desarrollo clínico
- Médico con formación en cirugía general
- Amplia experiencia en desarrollo clínico y aprobación regulatoria de Dispositivos Médicos
- Experiencia terapéutica en cardiovascular, respiratorio, oncología, diabetes y más

Djordje Lazovic
Cirujano ortopédico y profesor
- Profesor en la European Medical School Oldenburg-Groningen
- Especializado en cirugía de rodilla, endoprótesis y navegación quirúrgica
- Combina experiencia clínica con liderazgo académico en innovación ortopédica

Resultados probados en áreas terapéuticas
Desde cardiología y dispositivos vasculares hasta neurología y ortopedia, nuestro equipo CRO especializado genera evidencia clínica lista para la regulación que cumple los más altos estándares.
Casos de clientes
Casos de clientes recientes: resultados reales en áreas terapéuticas
Explora algunos de nuestros estudios y proyectos recientes, desde SaMD e insuficiencia cardíaca hasta ictus y artrosis.
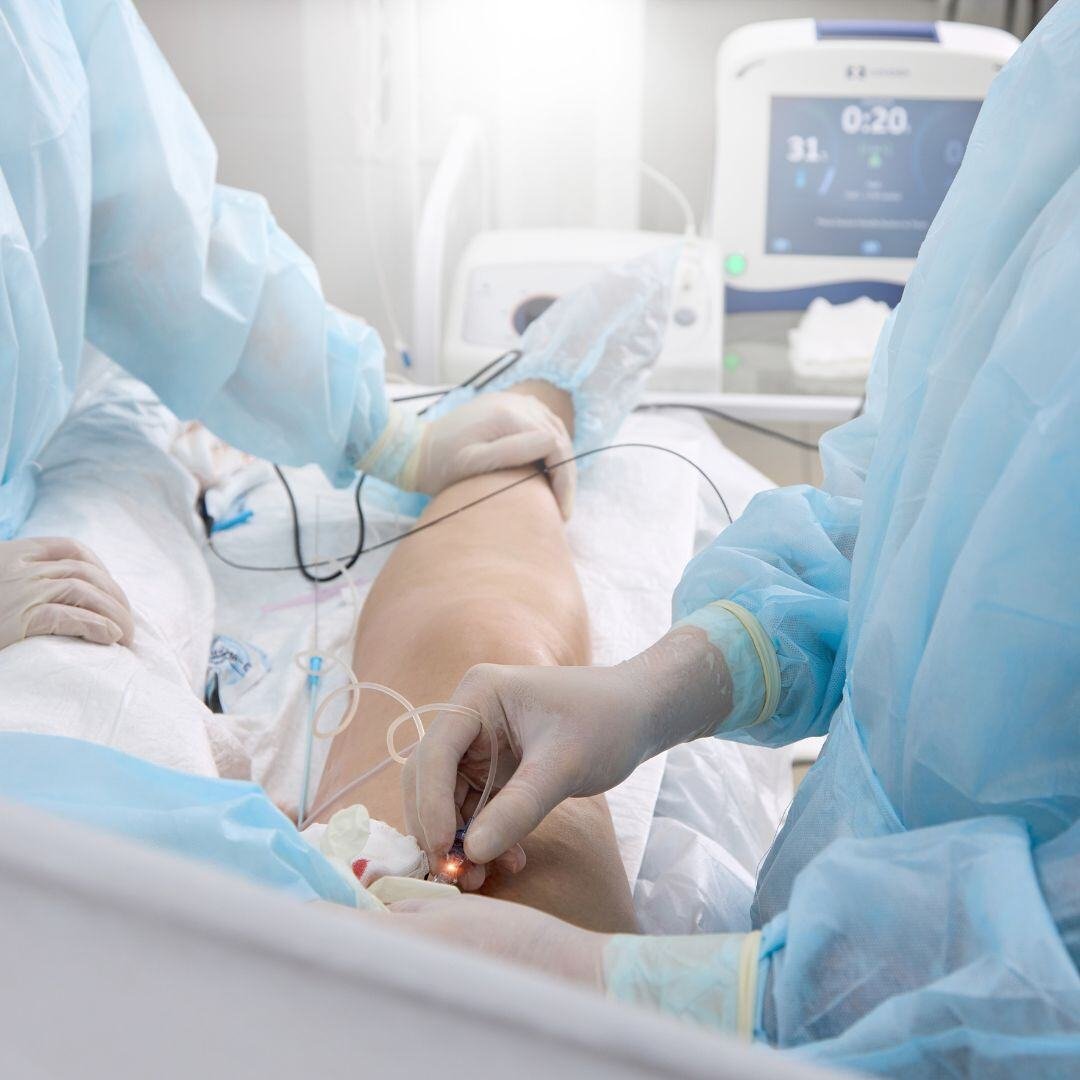 Vascular
VascularVascular | SaMD
Soporte a un registro poscomercialización de 5 años para SaMD de enfermedad arterial coronaria en 4 centros en Oriente Medio, Europa y EE. UU. Supervisión completa del proyecto, gestión de centros y soporte de recursos locales para 394 sujetos.
 Cardiology
CardiologyCardio | Insuficiencia cardíaca
Gestión de un estudio de seguimiento First-in-Human para tecnología de microordenador intracardiaco dirigido a la enfermedad cardíaca isquémica. En 12 centros en Europa y Oriente Medio con 30 sujetos, proporcionamos presentaciones regulatorias, monitorización y consultoría MDR.
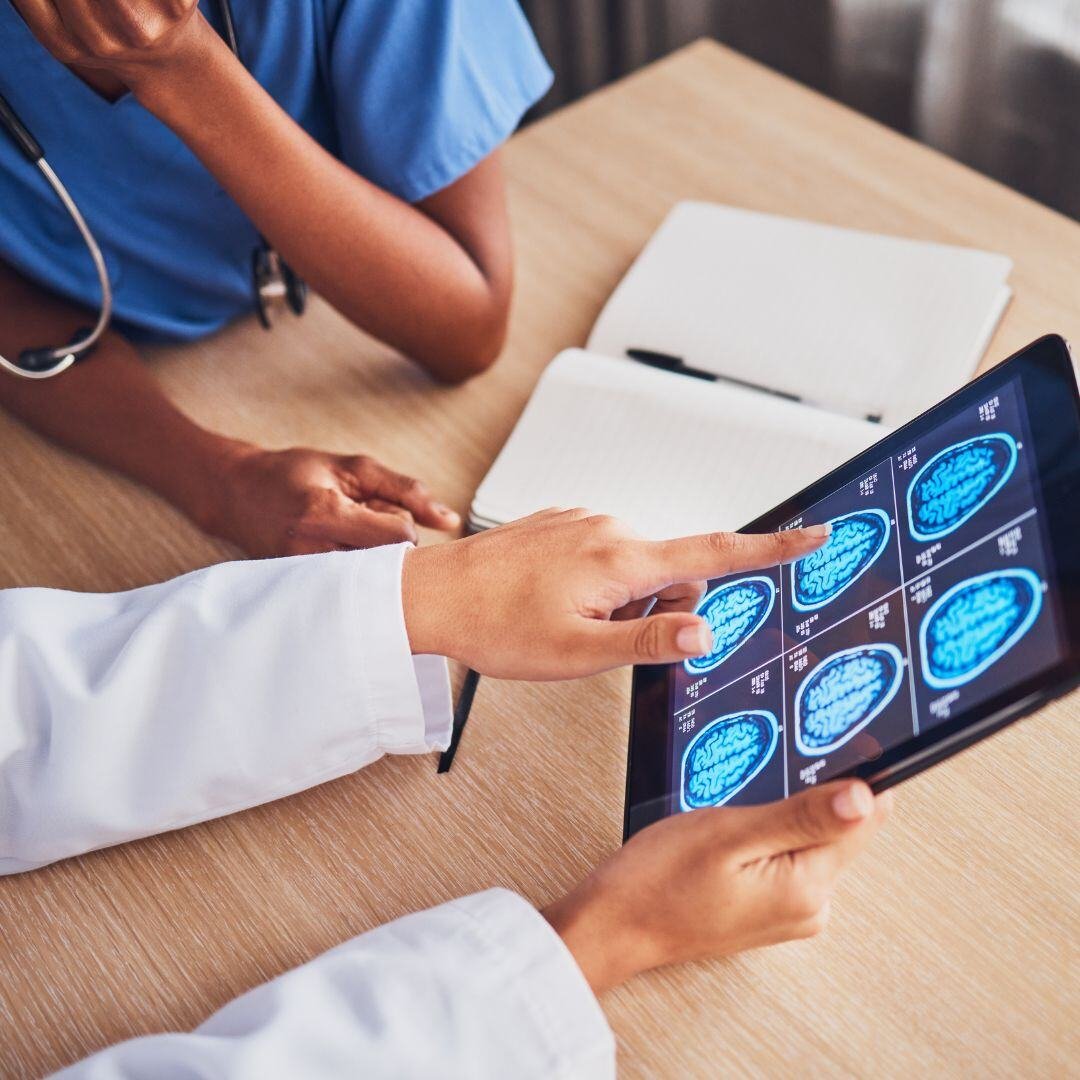 Neurology
NeurologyNeuro | Ictus
Dirección de un estudio intervencionista pivotal en la UE y EE. UU. para catéteres de aspiración relacionados con el ictus. Previsto para 277 sujetos, nuestros servicios CRO completos incluyeron presentaciones, bioestadística y gestión de datos.
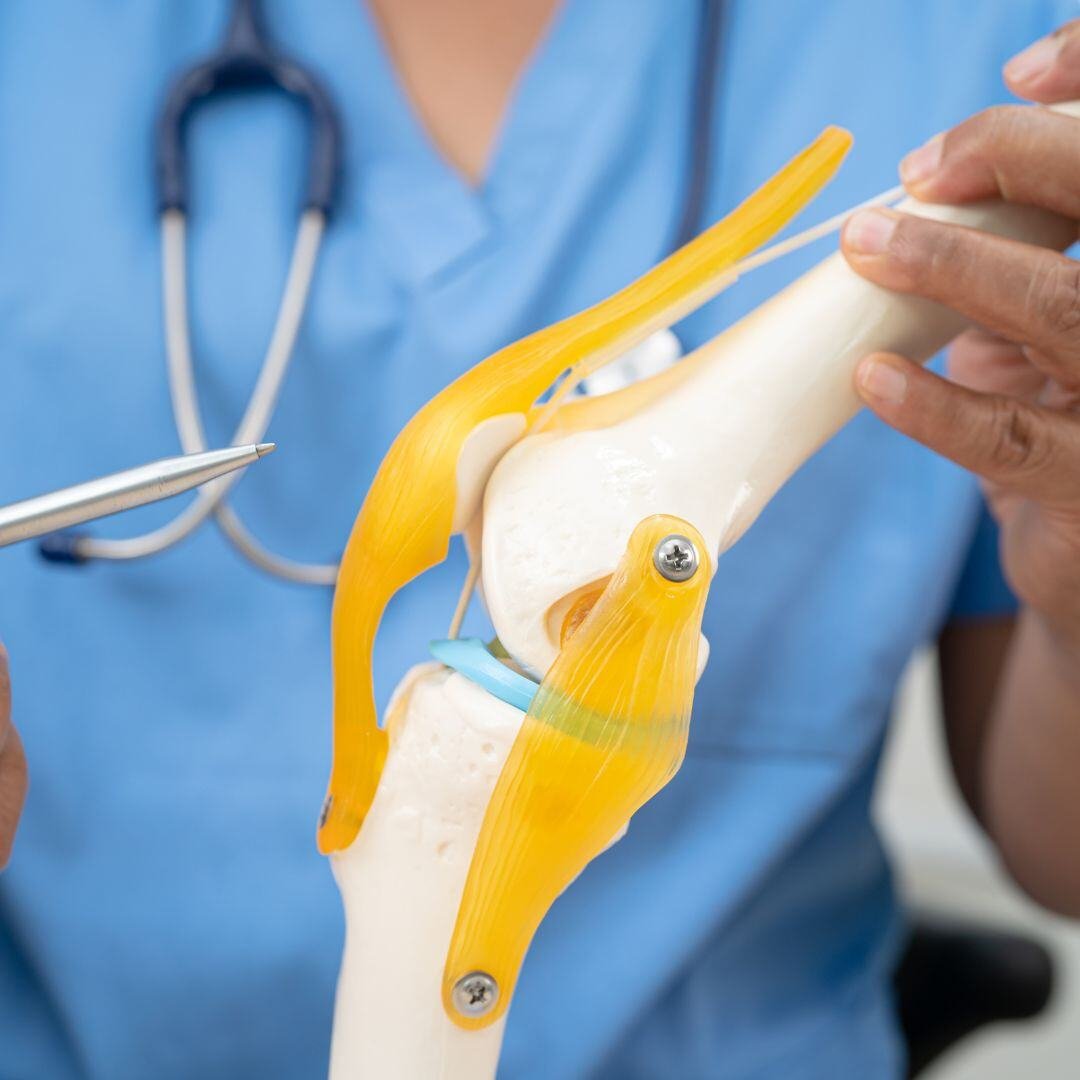 Orthopedic
OrthopedicOrtopedia | Artrosis
Supervisión de un estudio inicial First-in-Human para inyecciones de hidrogel intraarticular para el tratamiento de la artrosis de rodilla. Realizado en hasta 6 centros en Bélgica, con soporte completo de redacción médica, bioestadística y monitorización de seguridad para 99 sujetos previstos.

Por qué QbD Group
Tu socio de confianza
We support MedTech companies with regulatory expertise across MDR, FDA, IVDR, ISO 14155, ICH-GCP, and our close collaboration with Notified Bodies, enabling trust, transparency, and faster outcomes.
MedTech expertise
focused exclusively on medical devices, IVD and companion diagnostics.
Trusted partner
proven track record with innovators and established MedTech companies alike.
Quality at every step
rigorous processes ensure clinical evidence that meets regulatory expectations.
Right-sized solutions on budget
we scale our services to match your project needs and timeline.
FAQ
Lo que debes saber

Plan your clinical pathway
From gap assessment to full CRO delivery, our clinical experts are ready to support your MedTech journey.