
全方位医疗器械 CRO
QbD Clinical 是一家专门服务于医疗器械公司的全方位 CRO。从早期可行性研究和先导研究,到覆盖欧洲、北美和亚太地区的全球临床试验,以及上市后临床随访 (PMCF) 研究,我们陪伴申办方按时、按预算地将安全有效的器械送达患者。
通过内部专长与可信赖的国际合作伙伴关系的结合,我们的客户在其临床研究的每一步都受益于我们团队的深厚专业知识。我们帮助申办方应对欧盟MDR和FDA要求,确保合规、高效且以患者为中心的临床研究与其市场准入战略保持一致。
无论您计划进行欧洲研究还是全球临床研究,我们都作为您从战略到执行的唯一合作伙伴,实现更清晰的沟通、更顺畅的运营和更快的结果。
我们的运营范围
全球覆盖
凭借遍布欧洲的办事处和值得信赖的国际合作伙伴网络,我们在全球范围内支持医疗器械临床研究——从研究启动到关闭。
QbD团队直接覆盖
比利时、波兰、荷兰、卢森堡、法国、英国、德国、西班牙、奥地利、瑞士
通过首选合作伙伴和供应商
可通过供应商和合作伙伴扩展
我们如何帮助您?
核心治疗领域
我们支持医疗器械制造商在多个治疗领域,帮助他们为欧盟MDR合规(包括遗留设备的MDR过渡)和全球市场准入生成强有力的临床证据。
除了我们在欧盟监管途径方面的深厚经验外,我们还提供FDA申报的战略和运营支持,包括预提交、510(k)和PMA申请。我们对临床研究保持全面的欧洲监督和管理,确保各地区的高质量执行和监管准备。
神经病学
神经设备、卒中技术和神经监测解决方案专长。
骨科
骨科植入物、肌肉骨骼设备和康复技术研究。

从战略到执行的唯一CRO合作伙伴
我们引导医疗器械申办方应对欧盟MDR和FDA要求,确保合规、高效且以患者为中心的临床研究与您的市场准入战略保持一致。
为什么选择我们
为什么选择 QbD Clinical 作为您的医疗器械 CRO?
一家专为医疗器械临床研究的复杂性与法规要求而打造的专属 CRO。
深耕医疗器械领域
我们专注于医疗器械——涵盖 Class I 至 Class III、有源植入物和 SaMD,不会因 pharma 项目而分散精力。
法规实力
我们的内部专家帮助您在所有目标市场遵循 EU MDR、ISO 14155、GCP、GDPR 及当地法规。
全球试验执行
在欧洲、北美和 APAC 开展医疗器械试验经验丰富,并在全球拥有值得信赖的研究中心网络。
灵活、可扩展的合作模式
我们的模块化 CRO 服务可随项目规模灵活扩展——从早期可行性研究和启动到关键性试验及上市后随访。
深度协作
我们与您的内部团队或 OEM 合作伙伴无缝协作,最大化效率与成果。
我们的团队
认识我们的专家
进行医疗器械临床试验需要法规洞察力、临床专长和对设备特定要求的深刻理解的独特组合。

Dr. Diane Fairweather
全球临床部门负责人
20多年临床研究领导经验。
- 在临床研究和医疗器械开发方面拥有 20 多年经验
- 对全球临床项目进行战略监督
- 在 EU MDR、FDA 及国际监管框架方面拥有深厚专长

Julie Hendrickx
MD CRO项目管理主管
20多年临床项目交付经验。
- 在 Pharma 与医疗器械领域拥有国际经验
- 拥有 8 年以上临床项目经理经验
- 负责从研究启动到关闭的全流程项目管理

Petra De Geest
医学事务业务部门经理
12年医疗器械领域经验。
- 医疗器械临床证据与医学写作(Class I 至 Class III,包括 MDSW 及 AI 驱动的 MDSW)
- 医疗器械临床研究中的安全管理
- 战略领导与咨询服务
顾问委员会
认识顾问委员会
我们的医学顾问委员会汇聚了经验丰富的生命科学专业人士,在临床战略、患者安全、科学严谨性和法规合规方面提供专家指导。

Pierfrancesco Agostoni
介入心脏病专家
- 在侵入性与介入心脏病学领域拥有 20 多年经验
- 每年开展 300–400 例复杂 PCI 及约 80 例 TAVI 手术
- 擅长 CTO 介入、桡动脉入路及高级经皮技术
- 在 PubMed 收录刊物发表 310 余篇论文,撰写 10 余个书籍章节

Djordje Lazovic
骨科外科医生与教授
- European Medical School Oldenburg-Groningen 教授
- 专长于膝关节手术、人工关节置换及手术导航
- 将临床专业能力与骨科创新中的学术领导力相结合

各治疗领域的卓越成果
从心脏病学和血管设备到神经病学和骨科,我们专业的CRO团队提供符合最高标准的监管就绪临床证据。
客户案例
近期客户案例:各治疗领域的真实成果
探索我们近期的研究和项目,涵盖SaMD和心力衰竭到卒中和骨关节炎。
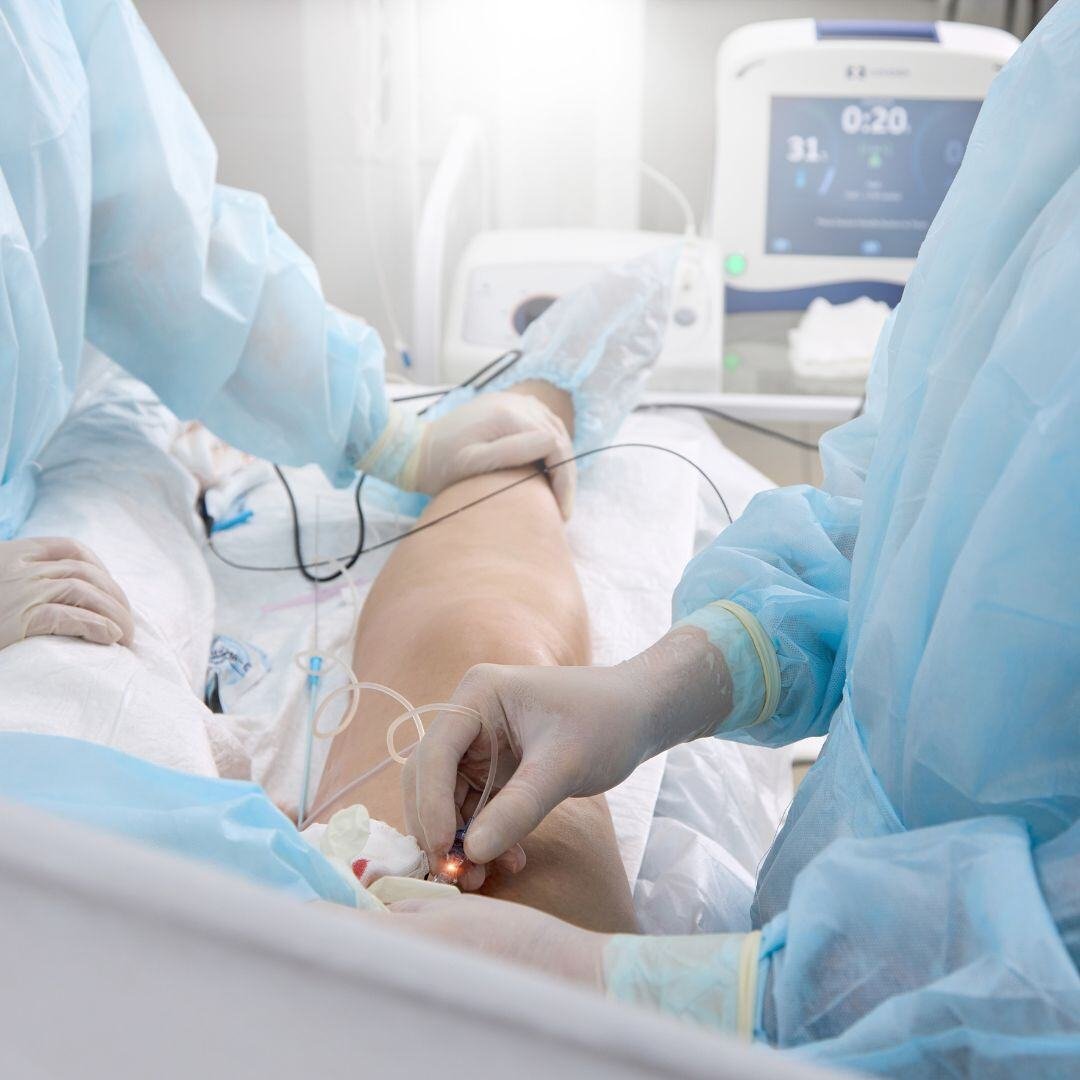 Vascular
Vascular血管 | SaMD
支持了一项为期5年的冠状动脉疾病SaMD上市后注册研究,覆盖中东、欧洲和美国的4个站点。为394名受试者提供了全面的项目监督、站点管理和本地资源支持。
 Cardiology
Cardiology心脏 | 心力衰竭
管理了一项针对缺血性心脏病的心脏内微型计算机技术首次人体随访研究。覆盖欧洲和中东12个站点,30名入组受试者,提供了监管申报、监查和MDR咨询。
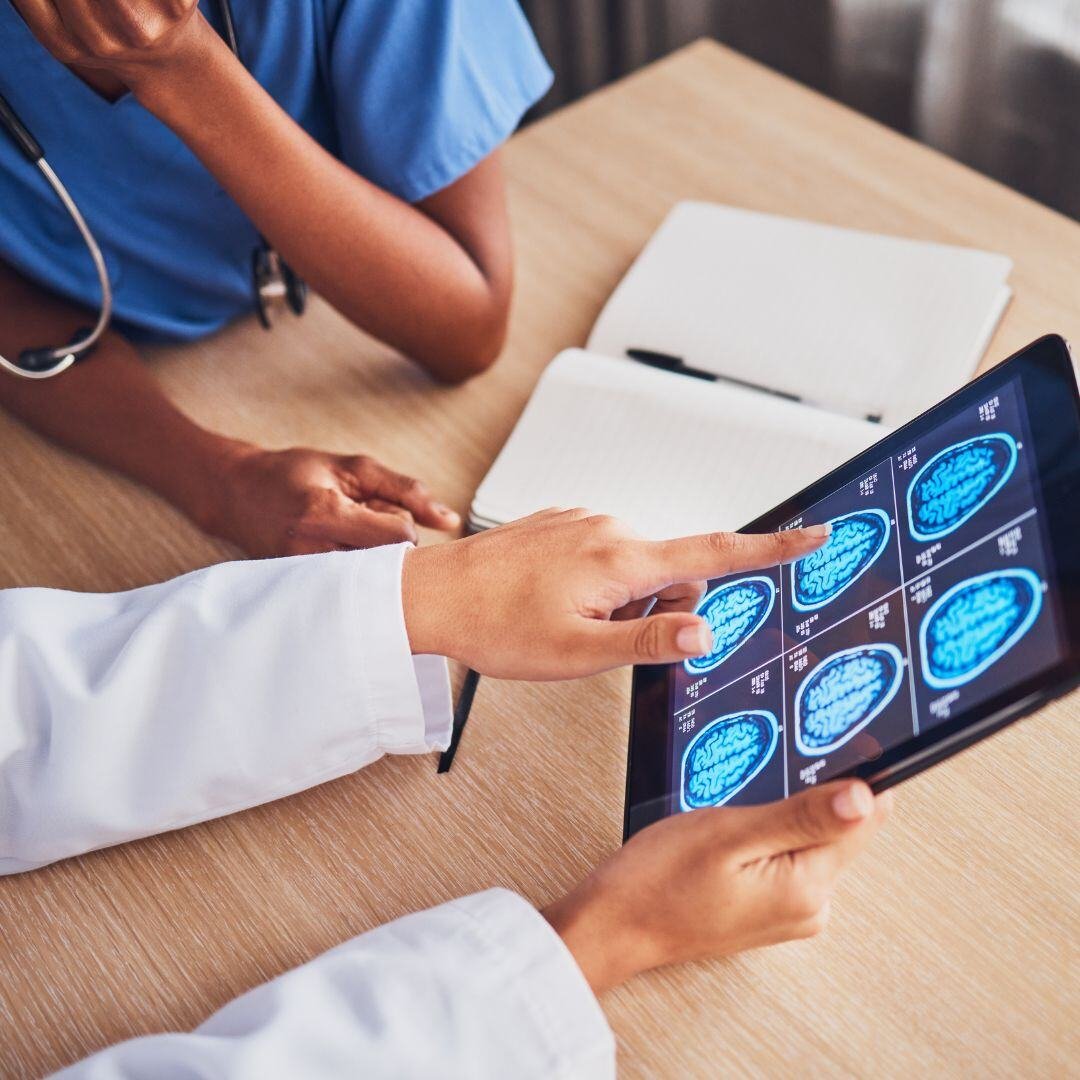 Neurology
Neurology神经 | 卒中
在欧盟和美国领导了一项针对卒中相关抽吸导管的关键介入研究。预计277名受试者,我们提供了全面的CRO服务,包括申报、生物统计和数据管理。
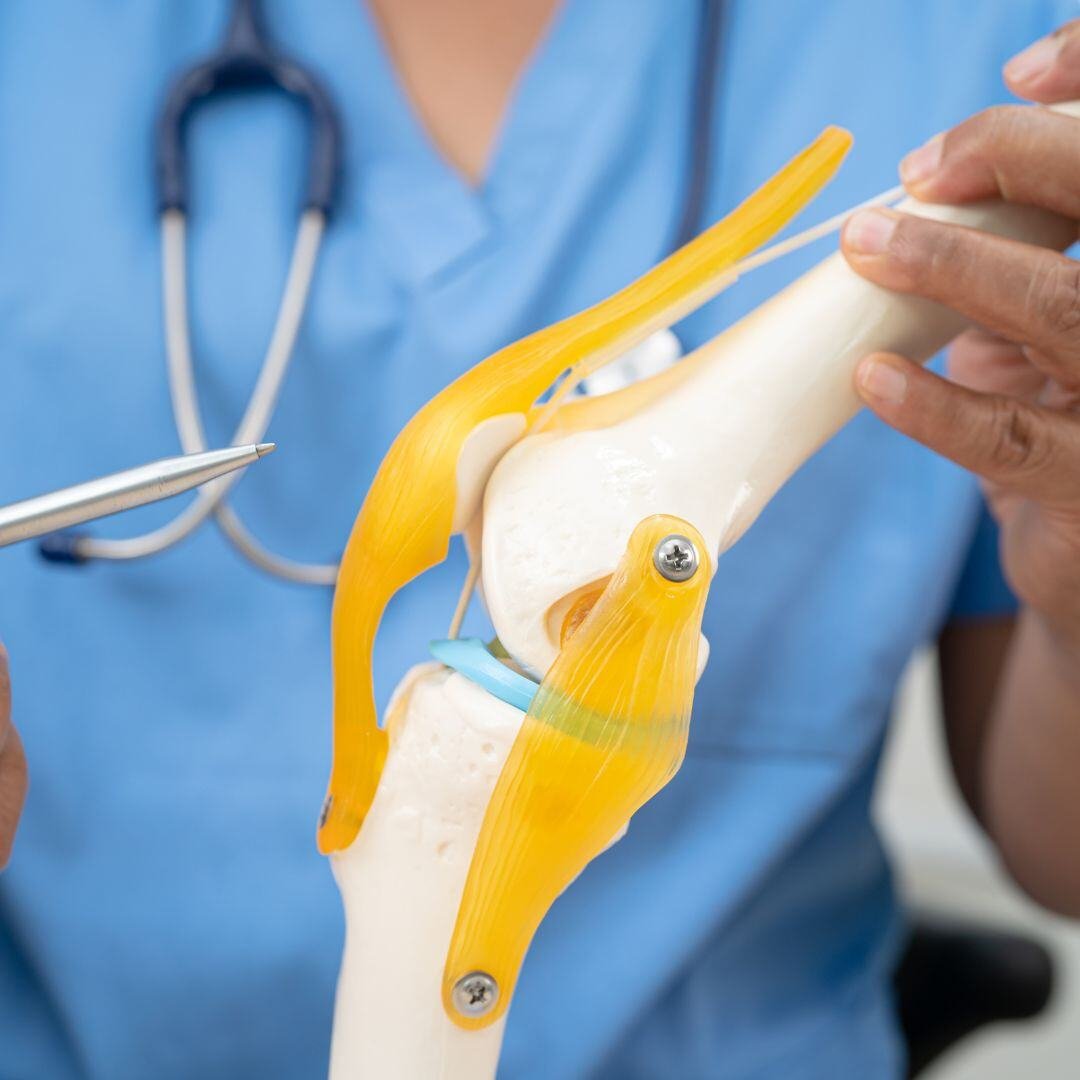 Orthopedic
Orthopedic骨科 | 骨关节炎
监督了一项用于治疗膝关节骨关节炎的关节内水凝胶注射首次人体启动研究。在比利时最多6个站点进行,为99名预计受试者提供了全面的医学写作、生物统计和安全监测支持。

为什么选择QbD Group
您值得信赖的合作伙伴
We support MedTech companies with regulatory expertise across MDR, FDA, IVDR, ISO 14155, ICH-GCP, and our close collaboration with Notified Bodies, enabling trust, transparency, and faster outcomes.
MedTech expertise
focused exclusively on medical devices, IVD and companion diagnostics.
Trusted partner
proven track record with innovators and established MedTech companies alike.
Quality at every step
rigorous processes ensure clinical evidence that meets regulatory expectations.
Right-sized solutions on budget
we scale our services to match your project needs and timeline.
FAQ
您需要了解的内容

Plan your clinical pathway
From gap assessment to full CRO delivery, our clinical experts are ready to support your MedTech journey.

