
药物-器械组合产品
自信导航欧盟和美国法规路径
导航法规路径常常感觉像是在迷宫中穿行,导致递交过程中的不确定性和潜在错误。对于组合产品来说更是如此。在QbD Group,我们提供全面的解决方案,帮助导航这些创新产品在欧盟和美国的复杂注册过程。
法规框架
在欧洲,组合产品根据其主要作用机理(PMOA)进行监管——产品主要作为药物产品还是医疗器械。这决定了适用的法规路径。
我们解决的关键挑战
PMOA识别
确定主要作用机理定义了整个法规路径和所需的档案。
跨类分类
组合产品在药物和器械框架之间运作,需要双重法规协调。
不同的法规框架
欧盟和美国对组合产品的分类和审批采用根本不同的方法。
复杂的递交要求
整合的法规档案必须满足多个监管机构的要求。
器械主导的组合产品
如果您的产品被分类为含辅助药物物质的医疗器械,则必须符合欧盟MDR 2017/745。
示例
药物洗脱支架 → 器械路径(MDR + EMA意见)
涂层导管 → 器械路径(MDR)
药物主导的组合产品
如果您的产品主要是药物产品,则组合在药物产品指令(2001/83/EC)下监管。
示例
预充式注射器 → 药物路径(DPM)
避孕贴 → 药物路径(DPM)
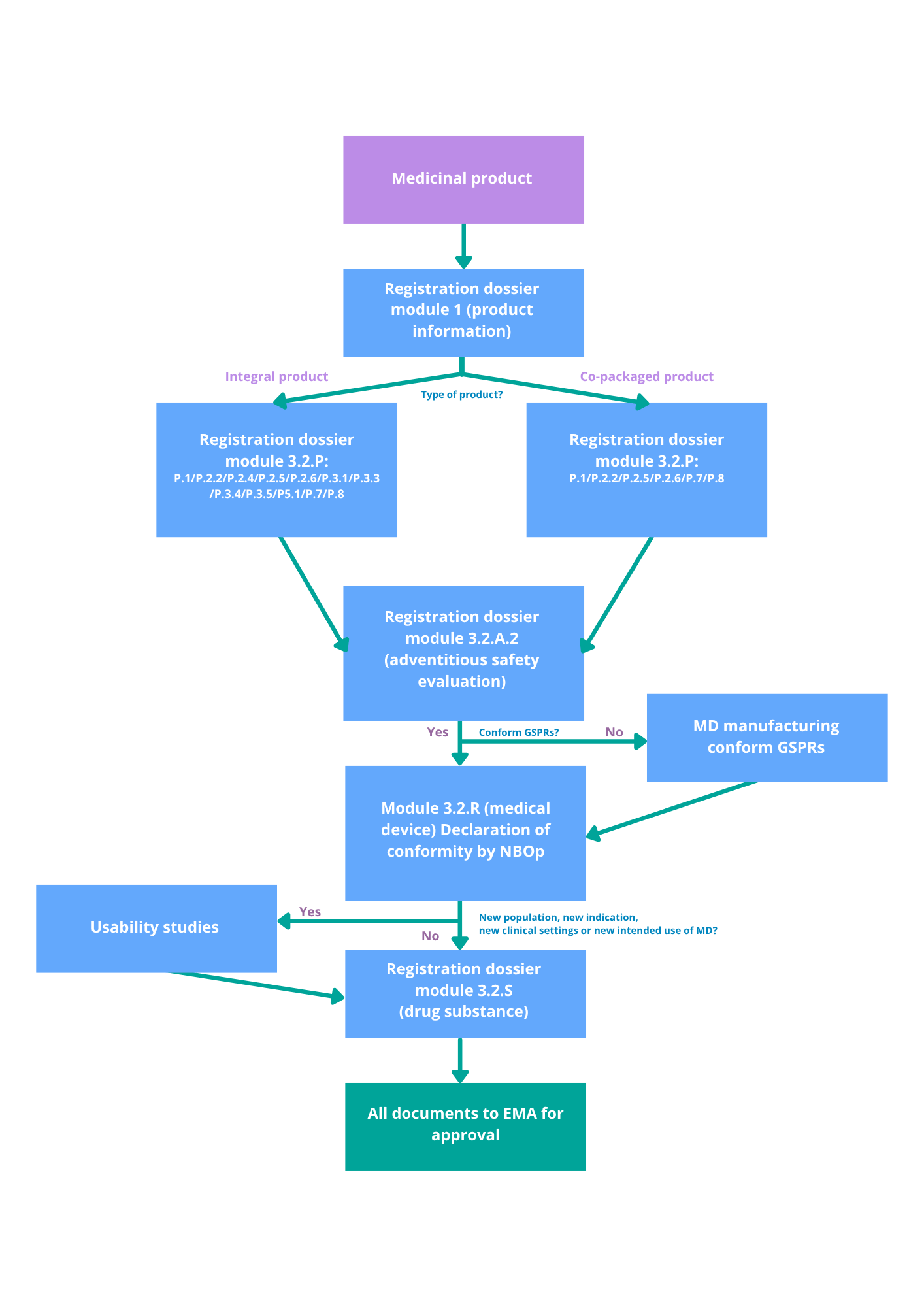
我们的结构化方法
确定FDA主导中心
确定主要作用机理(药物、器械或生物制品)。如不确定,向FDA提交指定申请(RFD)。
确定研究申请
根据PMOA,药物或生物制品主导时申请IND,器械主导时申请IDE。
选择上市申请
药物主导:NDA或ANDA。生物制品主导:BLA。器械主导:PMA、De Novo或510(k)。
上市后生命周期管理
在两个法规框架下保持持续合规。
我们的综合服务
我们的综合服务支持组织在整个运营生命周期中,从合规活动到持续控制、改进和数字化赋能。
你将获得
量身定制的法规策略
我们帮助您制定个性化的法规路径图。
专家程序指导
我们的团队引导您选择最合适的法规程序。
全面的生命周期管理
从概念到市场发布,我们提供全方位支持。
深厚的法规知识
利用我们广泛的专业知识自信地导航严格的要求。
为什么选择QbD Group
您值得信赖的合作伙伴
跨领域专业知识
—我们的法规专家在同一屋檐下覆盖制药、生物技术、医疗器械、IVD和组合产品。
战略法规规划
—我们将您的法规路径与商业目标对齐以加速上市。
经验证的业绩
—数千次成功递交和遍及欧洲的档案管理项目。
可扩展支持
—从一次性法规咨询到全面外包的法规运营。
常见问题
常见问题
