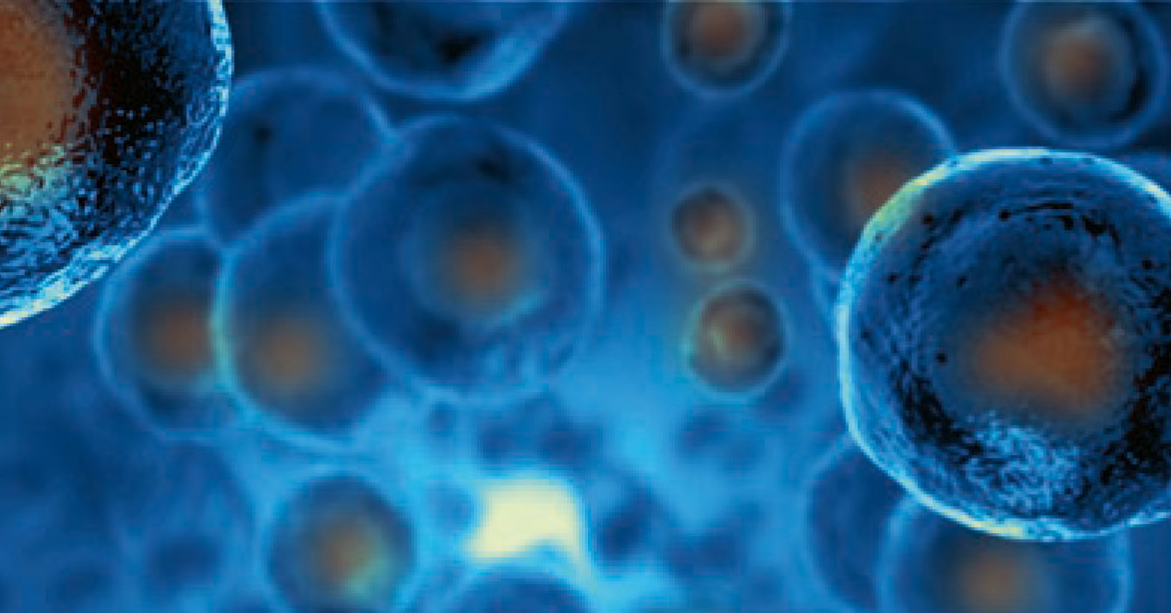
Todo lo que necesita saber sobre los ATMP: FAQ
¿Cuál es la definición de ATMP? Del sitio web de la EMA: Los medicamentos de terapia avanzada (MTA) son medicamentos de uso humano basados en

¿Cuál es la definición de ATMP? Del sitio web de la EMA: Los medicamentos de terapia avanzada (MTA) son medicamentos de uso humano basados en
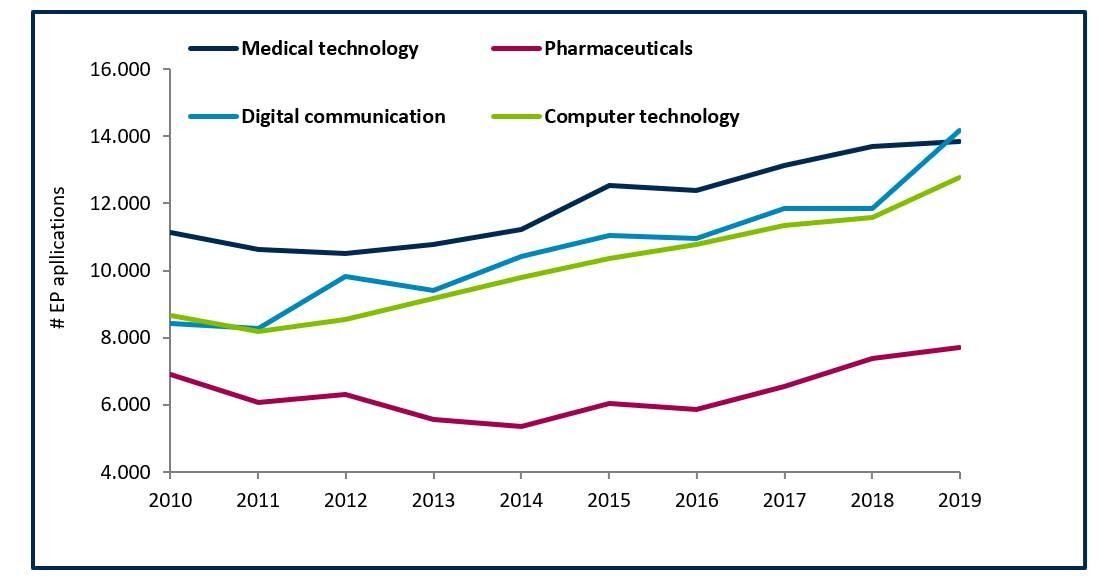
La innovación es la clave del éxito de las empresas y es el motor de muchas industrias. Esto es ciertamente cierto para el sector de

Hasta ahora, el mundo académico y las empresas basadas en la investigación han sido la principal fuente de desarrollos exitosos de ATMP (terapia génica y productos de ingeniería celular o tisular). Basándose en su éxito, las empresas farmacéuticas están intentando
El siguiente episodio del programa de conferencias invitadas para los estudiantes de Ingeniería Biomédica de la Universidad de Lieja fue una nueva experiencia tanto para

¿Una congelación de la contratación durante Corona? ¡No puede ser! Aunque la crisis actual ha creado nuevos e inesperados retos, QbD no es el tipo

En el primer blog hablamos de las definiciones de validación y sistemas informáticos. La comprobación de la aptitud del sistema consiste en verificar si el sistema funciona de acuerdo con las necesidades del proceso para el que se adquiere.

Como saben, QbD es una organización muy deportiva y saludable. Como hoy empieza la semana 2 de deberes y distanciamiento social, obviamente echamos de menos

¿Comprobando su teléfono para ver cuándo tomó su última medicación? ¿Su reloj vibrando y diciéndole que se acueste porque va a tener un ataque pronto, mientras que al mismo tiempo notifica a su contacto de emergencia con su ubicación exacta?

El lunes 27 de abril, los estudiantes de Ingeniería Biomédica de la Universidad de Lieja asistieron a la cuarta conferencia invitada de QbD. En esta ocasión, Bart Verlinden y Pieter Smits, responsables de QbD, introdujeron a los estudiantes en el software como dispositivo médico y en la validación y cualificación.

Como Ingeniero de Apoyo a la Producción doy soporte a mi cliente Biocartis con problemas asociados al proceso de producción. Dependiendo del problema, mi trabajo
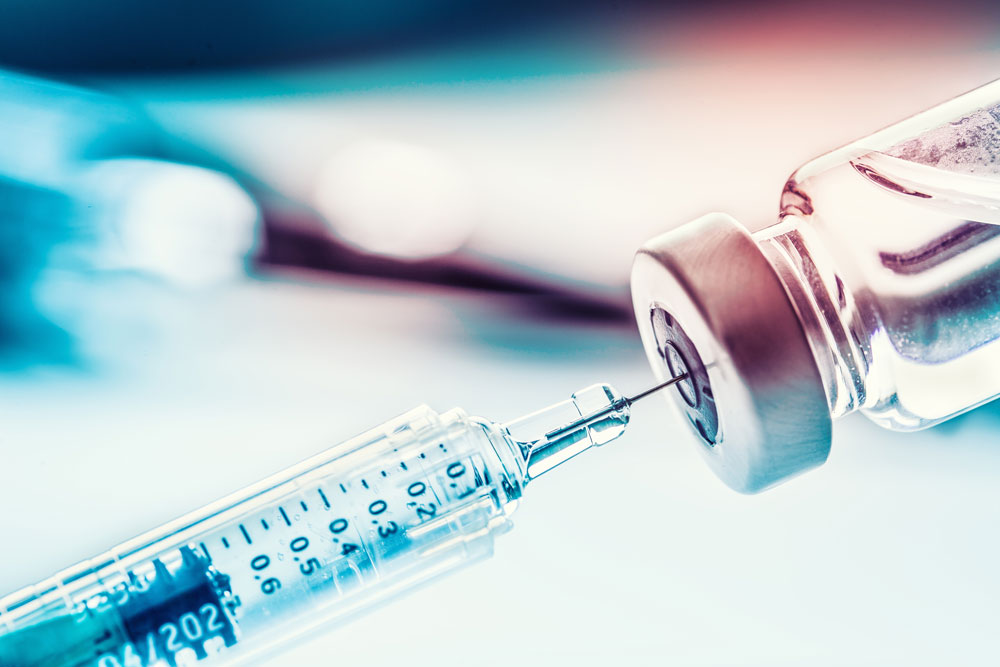
Cuando se trata de la salida al mercado de las vacunas, hay algunos requisitos y legislaciones específicas que las empresas deben tener en cuenta. En esta entrada del blog, prestaremos atención a la salida al mercado de las vacunas en dos de los mercados más importantes del mundo: la Unión Europea y los Estados Unidos de América. Aunque son bastante similares, hay algunas diferencias interesantes en lo que respecta a las pruebas, la documentación y la certificación.
Los países dependen del uso de dispositivos médicos para lograr la cobertura sanitaria universal, responder a las emergencias sanitarias y mantener la seguridad de la

El reloj está en marcha para el Brexit. Antes del 31 de octubre de 2019, debe alcanzarse un acuerdo definitivo al respecto. No cabe duda de que la salida del Reino Unido de la Unión Europea (UE) tendrá un enorme impacto en el Reino Unido y en los Estados miembros de la UE.

¡Es hora de invadir la privacidad de otro QbDer! En su “Día en la vida de QbD de…”, Lieve De Wolf nos acerca a un

Ha llegado el momento de echar un vistazo al día a día de otro de nuestros QbD’s. Conoce a Julie Bondroit, una de las integrantes

Cómo la QbD pone el “juego” en el “trabajo, juego, entrega” – parte 1 Hace tiempo, Martijn, uno de los socios gestores de QbD, tenía

Respaldado por las crecientes inversiones de los patrocinadores comerciales, el desarrollo de medicamentos de terapia avanzada (ATMP) está creciendo con fuerza en el Reino Unido.

Imagina que le explicas el uso de Excel y todas sus funciones a alguien que nunca ha trabajado con el programa, en un manual escrito.

El grupo de calificación y validación dentro de QbD organizó su primera Centro de Competencia hace unas semanas. Este foro se utiliza para debatir temas

¿Quiere saber cómo es un día típico de trabajo en Quality by Design? En la primera parte de nuestro nuevoSerie de blogs “Un día en

La QbD es conocida por su espíritu de equipo y su carácter deportivo. Esto no sólo ocurre en la oficina, sino también fuera del trabajo.

La falsificación siempre ha sido un problema importante. Aunque puede parecer un buen negocio cuando se puede encontrar su marca favorita de bienes de consumo

Allí estábamos, en el “quartier Polytech”, buscando el departamento “Aérospatiale & Mécanique” de la universidad de Lieja. Nos habíamos levantado demasiado temprano, pero una pequeña

sta semana, la farmacéutica Evelyne Goudezeune nos trae un típico “Día en la vida de la QbD”, lleno de varias reuniones y una velada muy entretenida. ¿Te gusta lo que lees? Entonces asegúrate de enviarnos tu cv para unirte a nuestro increíble equipo

Tras meses de revisión y muchas preguntas planteadas, parece que ha llegado el momento de aplicar los nuevos requisitos contenidos en la revisión del anexo

Los medicamentos de terapia avanzada (ATMP) son terapias celulares y genéticas que ofrecen nuevas oportunidades para el tratamiento de diversas enfermedades y lesiones. Debido a

La fabricación y venta de medicamentos es un gran negocio. En consecuencia, los medicamentos falsificados son una grave amenaza para los pacientes que dependen de

¿Se pregunta cómo es un día típico de trabajo en Quality by Design? En la segunda parte de nuestra serie de blogs “Un día en
Los productos sanitarios desempeñan literalmente un papel vital en la sociedad. Como son clave para curar a los pacientes y salvar vidas, están sujetos a

Cada día está más cerca una nueva era en la asistencia sanitaria. Gracias al cruce de Con la impresión 3D y la biología, las soluciones

En los últimos dos años, el tema de la integridad de los datos ha recibido cada vez más atención. Recientemente, la Administración de Alimentos y
El 26 de septiembre de 2012, la Comisión Europea adoptó una propuesta de reglamento del Parlamento Europeo y del Consejo, para revisar la legislación existente
Estos últimos días, la falta de regulación de los dispositivos médicos (MDR) en la Unión Europea ha sido destacada por muchos medios de comunicación. Como
En los últimos años, las técnicas de impresión en 3D han revolucionado el sector sanitario en todo el mundo. La impresión 3D tiene la capacidad
En los últimos años, las técnicas de impresión 3D han revolucionado la industria de la salud en todo el mundo. La impresión 3D tiene la
Varios avances científicos y clínicos de nuestra última década demuestran que los medicamentos de terapia avanzada (ATMP) revolucionarán la medicina del siglo XXI. Utilizando células
Por supuesto, es fundamental que las empresas de ciencias de la vida cumplan las normas de calidad más estrictas. Pero muchos otros sectores también están
El 20 de diciembre de 2017, la Agencia Europeade Medicamentos (EMA) publicó el borrador para el nuevo Anexo 1 de BPF de la UE “Fabricación
El panorama de los productos sanitarios está sometido a normas y reglamentos cada vez más estrictos. Aunque a veces se perciba como una molestia, lo
La integridad de los datos es la piedra angular del progreso científico. Sin embargo, un reciente artículo publicado en un importante periódico belga muestra que

Cada día, pacientes de todo el mundo participan en ensayos clínicos. Sus contribuciones son cruciales, ya que garantizan el progreso de una investigación vital. Sin
Recientemente, la MHPRA (Agencia Reguladora de Medicamentos y Productos Sanitarios) del Reino Unido publicó un documento de orientación sobre la integridad de los datos en
Han pasado más de 10 años desde la última revisión del anexo 1 de las PCF de la UE. El 20 de diciembre de 2017,
No hace falta preguntarle a Papá Noel por el PIB. Pregúntale a Sofie. El PIB cubre la crucial “última milla” después de la producción. Es
El Acuerdo de Reconocimiento Mutuo entre Estados Unidos y la Unión Europea está entrando en vigor gradualmente. Desde noviembre de 2017 la FDA reconoce a

La serialización está surgiendo rápidamente en el mundo farmacéutico. Para luchar contra la falsificación de medicamentos, cada vez más gobiernos exigen que cada producto de
Las formaciones especializadas son una manera de seguir invirtiendo en la experiencia de nuestro equipo de QbD. Tres colegas de QbD comparten sus opiniones sobre
El Acuerdo de Reconocimiento Mutuo entre Estados Unidos y la Unión Europea está entrando en vigor gradualmente. Desde noviembre de 2017 la FDA reconoce a
En un mundo cada vez más digital, el entorno sanitario se enfrenta a complejos retos. Está claro que las empresas sanitarias tendrán que adoptar sistemas
Cuando una instalación de GMP aprobada por las inspecciones de la FDA tenga problemas de incumplimiento, se le notificarán las medidas y los requisitos necesarios
A finales del año pasado, la ICH publicó la directriz armonizada sobre impurezas elementales. Esta directriz establece las PDE (Exposiciones Diarias Permitidas) de los elementos
45.000 euros. Es la multa que tienen que pagar las empresas farmacéuticas cuando no pueden suministrar inesperadamente ciertos medicamentos. La ministra holandesa de Salud Pública,
A principios de noviembre de 2015, emprendí un viaje de diez días a Escandinavia. ¿Propósito principal del viaje? Comprobación de una máquina de llenado y
La FDA publica un proyecto de guía “Buenas prácticas de fabricación actuales: Requisito para productos combinados“. En este momento, la revisión está pendiente, hasta el
“Opuestos”: esa es la palabra que me viene a la mente al recordar mi aventura de cuatro semanas de QbD en Estados Unidos. Extremos opuestos.
Cuando se dice farmacia, se dice cumplimiento. La introducción de nuevos productos farmacéuticos en el mercado está sujeta a normas muy estrictas sobre el desarrollo,
Dos directrices recientes de la FDA En 2016, la Administración de Alimentos y Medicamentos de los Estados Unidos publicó dos documentos de orientación muy diferentes
Para que pueda ver: la farmacopea japonesa y las normas GMP están disponibles en línea en el sitio web de la PMDA (Agencia de Productos
Dado que, con el paso del tiempo, los medicamentos destinados al mercado europeo se producen cada vez más fuera de Europa, la EMA quiere redactar
Como ingeniero de proyectos farmacéuticos en QbD, cada día es diferente. Más aún cuando se visita un país muy diferente al nuestro. El mes pasado
Archivo maestro de sustancias activas Los pacientes conocen el DMF, o Drug Master File, un documento en el que se proporciona toda la información sobre
USP ha publicado en su página web 5 borradores de artículos, entre ellos las Buenas Prácticas de Distribución (GDP) https://www.usp.org/usp-nf/notices/additional-feedback-sought-proposed-storage-and-distribution-general-chapters. Estos objetivos se basan en
Con la llegada del invierno, ha llegado el momento de vacunarse contra la gripe. Muchas personas, a menudo mayores de sesenta años o con una
En los últimos tres años, la industria de las ciencias de la vida ha creado entre 3.000 y 3.500 puestos de trabajo adicionales en Bélgica.
Nuevo Capítulo 2 Personal La EMA no ha dejado de lado los últimos meses en lo que se refiere a su sistema de GMP. El
A principios de este mes, un equipo de QbD visitó las Jornadas Nórdicas de Ciencias de la Vida en Estocolmo (Suecia). El evento habría estado
QbD apoya el fuerte crecimiento de HistoGeneX optimizando los sistemas informáticos HistoGeneX recurre a la ayuda de Quality by Design, experto en garantía de calidad
Los últimos avances en el mercado de los medicamentos huérfanos son prometedores. Además de los Países Bajos y Luxemburgo, la ministra flamenca de Salud Pública,
El pasado mes de marzo, la Unión Europea publicó unas directrices actualizadas en el Eudralex – Volumen 4: Directrices sobre buenas prácticas de fabricación (GMP).

La elaboración de requerimientos de usuario es una actividad que por la importancia de los mismos al inicio y final del Modelo V necesita de

En primer lugar, es importante entender la relevancia de la calificación de personal tener en cuenta que los procesos de fabricación, calidad y control de

De acuerdo con la normatividad, la documentación es una parte esencial del sistema de gestión de calidad en la industria farmacéutica, y, por tanto, debe

A pesar de que la capacitación de personal es fundamental para el éxito de las empresas, algunas desafortunadamente la ven como una carga. Lo anterior,
¿Alguna vez te has preguntado sobre los requerimientos GMP que debe cumplir una planta de producción? En este blog te contaremos algunos temas que debes
En este blog te explicaremos de forma clara y sencilla el Plan Maestro de Validación (PMV). Aquí, aprenderás qué es, el porqué se realiza, qué
Los registros electrónicos son aquellos datos e información que se crean, modifican, archivan, recuperan y distribuyen mediante un sistema informático. Existen Registros Electrónicos de relevancia BPX y aquellos que no lo son, la diferencia radica en si impactan o no al cumplimiento
¿Conoces la importancia de determinar y analizar los riesgos del sistema? ¿En qué etapa del ciclo de la vida del sistema debemos realizar esta evaluación?
¿Qué es la infraestructura? La infraestructura de Tecnología de la información (TI) es la base que soporta las operaciones de las industrias, en ella se
Webinar sin costo de: Validaciones, integridad de datos, calificaciones, normas y mucho más: ¿Te gustaría obtener algún webinar completo sin ningún costo? Déjanos tus datos

Existen 6 tipos principales de impactos a considerar para los sistemas computarizados. Estos deberán de evaluarse tanto en los análisis de riesgos iniciales al sistema

¿Requieres apoyo en la implementación del decreto supremo 021-2018 “Manual de Buenas Prácticas de Manufactura de Productos farmacéuticos” de Perú? Para QbD es importante hablarles
Las 8 preguntas básicas de un estudio de Mapeo Térmico o Condiciones Ambientales. El mapeo térmico o de condiciones ambientales: es un proceso de registro

Este blog es la continuación de la primera parte que contiene otras 5 cosas importantes que debes conocer antes de iniciar por primera vez a

Buenas Prácticas de Manufactura: Informes de la OMS (32, 37 y 45) Es importante que sepan que no en todos los informes de la OMS

1.Define el equipo para validar sistemas A la hora de validar sistemas, esta es una de las primeras actividades que se deberán definir antes de

Estos son los aspectos importantes del mapeo de áreas controladas que queremos que conozcas. Te lo contamos todo aquí. Empezamos por algo importante y es

La configuración de hojas de cálculo es muy importante, ya que ayuda a tener mayor agilidad en nuestros procesos, evitando errores en el uso y

¿Qué es un ERP? Un ERP (Enterprise Resource Planning) es un software de gestión para administrar e integrar las actividades de finanzas, cadena de suministro,

Aspectos básicos e importantes para la calificación de equipos. La calificación de equipos es un proceso fundamental en las industrias farmacéuticas. Este permite demostrar que

¿Conoces la importancia de la validación de HVAC? Los cuartos donde se realiza la fabricación de medicamentos o insumos de la salud requieren ser controlados;

¿Alguna vez te has preguntado cuál es la frecuencia para realizar la calificación de equipos? Los equipos de producción y laboratorio requieren calificación y algunos

La cadena de frío se refiere a mantener las condiciones de temperatura necesarias para garantizar la calidad y seguridad de los productos a lo largo

El pensamiento crítico puede jugar un papel muy importante dentro de muchas actividades de cumplimiento regulatorio. Jaime Castro, profundiza mucho más este tema a través

¡México, te tenemos una increíble promoción! ¡Conoce aquí la promoción especial que tenemos para ti durante la temporada del Buen Fin 2020! En la compra
¡Inscríbete hoy a nuestro SEMINARIO sobre la nueva guía GAMP “Data Integrity by design”! Este apéndice detalla los conceptos claves de CSA (Computer System Assurance

Nos alegra contar con una nueva alianza: Quality by Design y TRIUM. Juntas, las empresas de consultoría de ciencias de la vida crean una oferta

Hoy queremos compartirte algunas preguntas de Auditoría en la Validación de Procesos, así que ¡prepárate! Muchas veces nos preguntamos que debemos conocer, tener a la

El pasado 16 de septiembre, una de las asociaciones del cannabis industrial colombiana presentó una carta formal al Gobierno Nacional, solicitando que considere regular la exportación

Evaluar impacto y análisis de riesgo, antes y durante el proceso de validación. En este blog te compartimos la importancia de evaluar impacto y análisis

Ya han pasado 12 años desde la creación de la guía GAMP 5 (c) de la ISPE y ¡La mayor parte de su contenido sigue vigente! Aun cuando con certeza
Come to see the QbD Group at stand #3G73 at CPHI Conference in Barcelona. And after the conference…Eat & Connect with lifescience professionals at our QbD’s CPHI Networking Drink.