
Asegurando la efectividad: Puntos clave para la calificación de autoclaves
¿Qué es una autoclave? Es un recipiente metálico de paredes gruesas con cierre hermético que permite trabajar con vapor de agua a alta presión y
QbD » Blog

¿Qué es una autoclave? Es un recipiente metálico de paredes gruesas con cierre hermético que permite trabajar con vapor de agua a alta presión y

El mapeo térmico es una técnica en la cual se utilizan sensores de condiciones ambientales para monitorear y registrar las variaciones en áreas específicas, esta

En life sciences, un sector cada vez más digitalizado, la incorporación de nuevas tecnologías además de ayudar a hacer más eficientes los recursos y los procesos, conlleva ciertas implicaciones en cuanto a riesgos que son inherentes a la digitalización de los procesos. Existen diversas razones por las cuales las empresas de life sciences son blanco de ataques cibernéticos y dependen de prácticas sólidas y medidas fuertes de ciberseguridad para protegerse contra las amenazas y garantizar un entorno digital seguro.

El Informe 37 de la OMS nos habla sobre las Buenas Prácticas de Manufactura en la industria farmacéutica. Se enfoca en la importancia de mantener estándares de calidad para garantizar la seguridad y eficacia de los medicamentos. Además, proporciona pautas clave como sanitización y validación para cumplir con los requerimientos de auditoría.

La validación de procesos de limpieza es crucial en las Buenas Prácticas de Manufactura (BPM) para asegurar la calidad consistente de productos farmacéuticos y prevenir la contaminación.

En este blog, hablaremos sobre el uso de los tanques en la industria según su tipología y de los documentos claves para su calificación.

En este blog, exploraremos la importancia de la cadena de frío y cómo la implementación de estos protocolos puede garantizar la integridad de los productos, así como la confiabilidad del proceso en su totalidad.

En este blog, podrás encontrar nociones básicas sobre la validación de hojas de cálculo.

En este blog, nos comprometemos a proporcionarte respuestas detalladas y explicaciones exhaustivas sobre las generalidades de la validación de sistemas computarizados. Además, abordaremos los requisitos necesarios para la validación de sistemas computarizados.

Este articulo proporciona orientación sobre la validación de un ERP (Enterprise Resource Planning) en el giro farmacéutico. Se discuten consejos prácticos, como la identificación de módulos con impacto en la calidad del producto, la integridad del paciente y la integridad de datos, así como la importancia de solicitar PNO’s o instructivos de los módulos con impacto.

La Revisión Periódica es un proceso de evaluación y mantenimiento que permite garantizar el funcionamiento adecuado y seguro de diferentes sistemas y servicios, identificando y corrigiendo problemas antes de que se conviertan en incidentes graves.

Mapeo Térmico: ¿Qué es? Es un proceso mediante el cual se recolectan o se registran datos de temperatura y/o humedad relativa de un espacio determinado,

En la industria farmacéutica se debe garantizar los procesos de producción y una tarea que hace parte de estos reglamentos es la calificación de equipos,

Descubre las últimas innovaciones en validación de sistemas informáticos con la segunda edición del GAMP 5. Como expertos en digitalización y validación, en este blog te contamos todas las novedades más destacadas que ofrece esta actualización. Optimiza tus procesos, garantiza la calidad y cumple con los estándares más exigentes de la industria de ciencias de la vida.

En sectores industriales regulados, hay una creciente demanda para registrar y supervisar en tiempo real las condiciones ambientales (como temperatura, humedad y presión). Esto garantiza

La mayoría de las empresas parecen no estar preparadas para afrontar con éxito una auditoría regulatoria que les permita obtener la certificación en BPx (buenas

La Revisión Anual del Producto (RAP) es el análisis histórico de la calidad de un producto, que toma como base todos los documentos normativos en uso en el ámbito farmacéutico (análisis de laboratorio, registros de producción, registros de incidentes, desviaciones, reclamaciones o quejas, devoluciones, etc.), los criterios reconocidos internacionalmente, así como las directrices internas de cada empresa.

¿Cuál es la importancia de la validación que va más allá de simplemente cumplir con las regulaciones? Si bien estamos conscientes de la necesidad de

¿Cuál es el propósito de la validación de una Hoja de Cálculo? La validación tiene como meta principal la generación de una evidencia documentada que

Backup: ¿Por qué se deben realizar? Las empresas que operan en sectores regulados, como el farmacéutico, el cannabis, las clínicas y otros, a menudo tienen

La Garantía de Sistemas Informáticos (CSA) consta en aplicar el pensamiento crítico en el proceso de validación para aplicar el nivel adecuado de pruebas a las actividades de mayor riesgo, con una disminución considerable del tiempo dedicado a la documentación, reduciendo así el esfuerzo de validación y centrando los esfuerzos en mejorar la calidad y el grado de cumplimiento de nuestros procesos empresariales.

Información en un procedimiento de operación (POS /SOP) En este artículo, proporcionaremos pautas sobre la información básica que debe incluir tu procedimiento de operación para

Consideraciones clave para evaluar el impacto de sistemas computarizados antes de validarlos Es esencial considerar varios puntos antes de iniciar la validación de sistemas computarizados

En este apartado, abordamos algunas de las preguntas que surgieron durante nuestro webinar online y gratuito sobre Mapeo térmico: ¿Qué se debe tener en cuenta

La validación sin papel llega al mundo de las ciencias de la vida, facilitando y otorgando nuevas herramientas que apoyarán la gestión documental (en todo su ciclo de vida), integridad de datos, automatización y eficiencia a través de la tecnología.

Explora la clasificación de sistemas informatizados y sus tipos basados en funcionalidad y diseño

El ciclo de vida de la validación de procesos es esencial para garantizar la calidad y la conformidad en la industria. Desde la planificación hasta la ejecución y el monitoreo, cada etapa juega un papel crucial en asegurar la eficiencia y la seguridad de los procesos de fabricación.

En el contexto de la auditoría de validación de sistemas computarizados, se revela la presencia constante de hallazgos recurrentes. En esta ocasión, Johana Sandoval, Gerente

En este apartado, abordamos algunas de las dudas que surgieron durante nuestro pasado webinar online y gratuito sobre Validación de hojas de cálculo dictado por

En la tercera parte de nuestra sobre Validación de procesos, te brindamos un completo análisis de la metodología de validación, criterios utilizados, conclusiones clave y

En nuestra segunda parte de la cápsula de validación de procesos, te presentamos información sobre la estructura del protocolo de validación, los pre requisitos necesarios,

En nuestro primer artículo de la capsula sobre las generalidades de la validación de procesos, exploraremos un poco sobre las BPM y su importancia en

¿Alguna vez te has preguntado en qué se basan los auditores para verificar la validación de hojas de cálculo? En este apartado, exploraremos las Normas

En la segunda parte de nuestra cápsula introductoria al Mapeo Térmico, exploraremos temas como la Etapa I, que abarca la elaboración de un protocolo y

En nuestra cápsula introductoria al mapeo térmico, parte 1, encontrarás información sobre la definición del tema, su alcance, las normativas asociadas, los objetivos y requisitos,

En este blog, te contaremos todo lo que necesitas saber sobre el software de gestión documental, como debe llevarse la documentación según el manual de buenas prácticas de manufactura y cómo puede beneficiar a tu empresa.

El artículo examina los principales impactos que pueden comprometer la integridad de los datos en sistemas computarizados. Se identifican cinco tipos de impactos y se enfatiza la necesidad de evaluarlos en los análisis de riesgos. Además, se explica cómo estos impactos pueden surgir y se resalta la importancia de preservar la integridad de los datos mediante atributos y buenas prácticas.

El mapeo de áreas controladas tiene puntos clave y esenciales que debes conocer. Nosotros te los contamos aquí.

Descubre los 8 puntos clave para verificar la calificación de personal y construir un equipo talentoso y eficiente en nuestro blog.

En este artículo siguiendo la GAMP 5, veremos la Calificación de instalación (IQ), y te daremos una lista de pruebas genéricas que te permitirá no olvidar ninguna prueba importante.

¿Estás seguro de saber qué sistemas computarizados necesitas validar?

¿Estás considerando validar tus sistemas computarizados? Antes de seguir adelante, es importante que conozcas algunos detalles clave que pueden ahorrarte tiempo, dinero y preocupaciones.

Es crucial entender lo que significa validar la limpieza, al igual que como debe hacerse, que áreas o equipos requieren de validación de limpieza y cuál es la manera correcta de documentarlo.

Te explicamos que debe tener el Plan Maestro de Validación de Sistemas computarizados y la importancia del mismo para cumplir la regulación.

Este Blog tiene como objetivo, comprender la importancia de un buen mantenimiento de un equipo en su ciclo de vida útil y consejos para ayudar a mantener sus condiciones de uso.

Mapeos térmicos y validación de cadena de frío Por: David Peña ¿Qué es? El mapeo térmico es el proceso por el cual adjuntas la evidencia

Validación de Métodos Analíticos Autor | Erick Miranda ¿Sabes que es validación de métodos analíticos? ¿Por qué validar métodos analíticos? ¿Para qué validar los métodos

El mapeo térmico o de condiciones ambientales: es un proceso de registro y de análisis de datos de temperatura y de humedad relativa de diferentes
El objetivo del Plan Maestro de Validación (PMV) específica y coordina todas las actividades de cualificación / validación con el propósito de asegurar que la
¿Qué son los Requisitos de Usuario? Los Requisitos de Usuario (RU´s o URS en inglés) son las expectativas que una organización tiene con respecto al
Imagínate explicándole el uso de Excel y todas sus funciones a alguien que nunca ha trabajado con el programa en un manual escrito. ¿Por dónde

En CSV, el desmantelamiento es la retirada o el cierre controlado de una solución informática o de un sistema informático que ya no es necesario. Conozca más sobre este proceso aquí.

Durante la pandemia, la firma electrónica adquirió una enorme importancia para las empresas del sector regulado. Conozca más sobre la firma electrónica, su uso y su seguridad aquí.

A veces es necesario realizar una migración de datos en sistemas informáticos, aplicaciones o software. Conozca más sobre el objetivo, la importancia y los riesgos aquí.

La calidad de los gases de proceso y de las redes de distribución de gases es cada vez más importante para los procesos farmacéuticos biotecnológicos y los centros ATMP. En este blog, destacamos la importancia de una red cualificada de gas de proceso y distribución, incluso en una fase temprana de desarrollo.

Este artículo se enfoca en el control estadístico de procesos y su importancia en la gestión de calidad empresarial, ofreciendo información sobre su implementación, herramientas y métodos, y destacando la relevancia del análisis de datos para la mejora continua.

¿Ha validado ya su(s) sistema(s) informático(s)? Entonces, las revisiones periódicas del CSV son un paso importante. Conozca más sobre su propósito y frecuencia aquí.
Preparación para la FDA Tras una inspección por parte de la FDA, el término “FDA readiness” es el más utilizado. Esto es muy sencillo: los
A pesar de que EMA lo ha mencionado en la sección de preguntas y respuestas, es un hecho que no se puede negar en la
ANDA significa “Abbreviated New Drug Application”. Una ANDA es un expediente que se presenta a la FDA para una variante genérica de un medicamento de
Aunque no se ha reducido la carga de trabajo de los usuarios y productores, la Agencia Europea del Medicamento (EMA) ha comenzado a revisar los
A principios de este año, la EMA publicó una revisión de las “Directrices sobre la aceptabilidad de los nombres de los medicamentos de uso humano”.
Hoy es San Valentín, por lo que quizás le hayan regalado un perfume u otro regalo de cosmética, o bien haya sorprendido a su pareja
Más inspecciones en todo el mundo Una noticia muy interesante, ya que la FDA ha aprobado un nuevo presupuesto más amplio que el anterior. Por
Nueva guía para la validación de métodos analíticos La FDA ha publicado una nueva Guía de Validación de Métodos Analíticos. Esto significa que el anterior,
Para la interpretación de los dos primeros artículos de este mes, consulte el artículo 3: Consideraciones generales para el cumplimiento de las CGMP: A. Demostrar
La última parte del borrador de las directrices de la FDA para los productos combinados, con una descripción detallada de los dos últimos artículos. Ficha
El concepto de Validación de Sistemas Informáticos hasta ahora nos ha servido bien y nos ha proporcionado la base de donde estamos hoy. Pero en

Validación de procesos La sección de validación de procesos ha doblado su tamaño de 2 a 4 páginas, con secciones adicionales sobre la verificación
A partir del 1 de octubre de 2015, entra en funcionamiento la revisión del Anexo 15 de EudraLex Vol 4, calificación y validación. El anexo
Los laboratorios clínicos y patológicos de los Países Bajos están experimentando grandes cambios. Un número creciente de ellas solicita la acreditación del “Raad voor Accreditatie”

Las autoinspecciones o auditorías internas son una parte esencial de su SGC. Además de determinar si su SGC cumple las directrices y normas, puede beneficiarse de ellas de varias maneras. Permiten conocer mejor los departamentos, explicar a la gente por qué son necesarios determinados procesos de calidad, recopilar información útil para mejorar el SGC y disponer de una herramienta para comprobar su preparación para las auditorías externas.

En Bélgica, la publicidad de los medicamentos está sujeta a la legislación para garantizar el uso racional de los mismos. Cada empresa debe designar a un responsable de la información y la publicidad, que comprueba la conformidad de la publicidad.

El Reglamento de Dispositivos Médicos (MDR) (UE) 2017/745 y el Reglamento de Dispositivos In Vitro (IVDR) (UE) 2017/746 introdujeron una nueva función obligatoria en el artículo 15: la persona responsable del cumplimiento normativo o “PRRC”. ¿Se pregunta qué significa el papel de PRRC y dónde puede encontrar a la persona adecuada? Entonces, ¡siga leyendo!

El aire comprimido y otros gases de proceso se utilizan en muchos pasos diferentes durante la fabricación de productos farmacéuticos. Algunos ejemplos son el uso de aire comprimido en contacto directo con los productos para limpiarlos, airearlos o moverlos a través de los procesos o el uso de gases de proceso en bombas de fluidos que llevan los productos a través de los procesos de producción y llenado. Los gases comprimidos, como el nitrógeno o el argón, también pueden utilizarse para cubrir o rociar un producto. Los riesgos asociados a la utilización de estos gases dependen de la cantidad y el tipo de contacto con el producto y, sobre la base de esta evaluación de riesgos, debe establecerse un plan de seguimiento adecuado.

¿Está pensando en una apasionante carrera como consultor en ciencias de la vida, pero aún tiene dudas? En este artículo, desmontamos 6 mitos sobre la asesoría para ayudarte a decidir.

Para documentar la evaluación clínica de su dispositivo y sus resultados, hay que elaborar un informe de evaluación clínica o CER. Obtenga más información sobre este documento clave, su contenido, las lagunas y los obstáculos más comunes.

En el QbD Group queremos tener en cuenta la opinión de nuestros empleados. Por lo tanto, nuestra Junta de Embajadores fue elegida para representar la voz de todos los QbD’ers, dentro y fuera del grupo. Thomas Van Looy ha sido elegido como uno de nuestros embajadores para 2022. ¡Felicidades, Thomas! Como embajador, le encanta compartir sus experiencias con el Grupo QbD. ¿Quieres saber más sobre el trabajo #QbDream de Thomas? Entonces no se pierda la entrevista que le presentamos a continuación.

Se considera que un certificado de adecuación a las monografías de la Farmacopea Europea (CEP) emitido por la EDQM sustituye a los apartados correspondientes de la solicitud de autorización de comercialización que demuestran la calidad de las sustancias de uso farmacéutico. La inclusión de un PEC en un AMS simplifica el proceso de revisión para las autoridades y los procedimientos de presentación para la industria. Sin embargo, con los próximos cambios en la legislación farmacéutica de la UE, el procedimiento CEP puede estar en peligro. En esta entrada del blog, exponemos los posibles cambios en un futuro próximo.
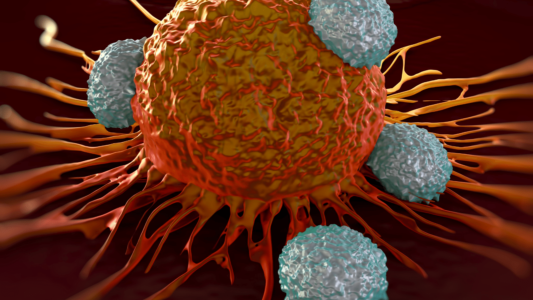
La terapia celular CAR-T utiliza células T modificadas genéticamente para destruir las células tumorales. Conozca los principales componentes, el proceso de fabricación y las perspectivas de esta prometedora inmunoterapia.

Steven Vinkx lleva 10 años trabajando para la QbD, y contando. Enhorabuena. ¿Tiene curiosidad por conocer su carrera y sus ideas? Entonces no deje de leer esta entrevista.
El 21 de agosto de 2022 entrará en vigor el nuevo Anexo 21 de las GMP. Este anexo contiene los requisitos de las prácticas correctas de fabricación para los titulares de MIA cuando importan medicamentos de fuera de la UE/EEE. Obtenga más información aquí.

¿Es usted un fabricante de productos sanitarios a medida y necesita orientación normativa? Este artículo resume las principales preocupaciones que hay que tener en cuenta.

El Plan de Evaluación Clínica, o CEP, es un punto de partida crucial y una guía para la evaluación clínica de su producto sanitario. Obtenga más información sobre este documento clave y sus requisitos.

Las categorías GAMP son muy importantes para decidir la estrategia de validación de su sistema informático. Conozca más sobre todas las categorías aquí.

La evaluación clínica de los productos sanitarios es fundamental para obtener y mantener la autorización de comercialización en la UE. Más información sobre la evaluación clínica aquí.

Dominiek Rossillion lleva 10 años trabajando en QbD, ¡y contando! Nuestra más sincera enhorabuena. ¿Tienes curiosidad por conocer la carrera de Dominiek y sus opiniones? Entonces no deje de leer esta entrevista.

En QbD, valoramos la opinión de nuestros empleados. Por ello, se formó la Junta de Embajadores de QbD para representar la voz de todos los QbD’s, en todo el Grupo QbD y más allá de las fronteras. Catarina Cruz ha sido elegida como una de nuestras embajadoras para 2022. Enhorabuena. Como embajadora, a Catarina le encanta compartir su experiencia de trabajo en QbD. ¿Quieres saber más sobre su trabajo #QbDream? No deje de leer la entrevista a continuación.

La nueva normativa sobre productos sanitarios y la correspondiente aplicación de EUDAMED pretenden dar al público en general acceso a la información pertinente sobre los productos sanitarios, garantizando una mayor transparencia. Sin embargo, EUDAMED también aporta nuevos requisitos para los participantes en el mercado a lo largo del ciclo de vida de los productos sanitarios. Lea más sobre ellos aquí.

En el QbD Group, la opinión de nuestros empleados es importante. Por ello, formamos una Junta de Embajadores para representar la voz de todos los QbD’ers, dentro y fuera del grupo. Marijn Bollema ha sido elegida como una de nuestras embajadoras para 2022. ¡Felicidades! Como embajador, Marijn quiere mostrar al mundo lo que es ser un verdadero QbD. ¿Quieres saber más sobre su trabajo #QbDream? No deje de leer la entrevista a continuación.

Los asuntos reglamentarios desempeñan un papel fundamental en la industria farmacéutica: desde el desarrollo del medicamento hasta su comercialización. Obtenga más información sobre los papeles y las funciones que los equipos de AR pueden proporcionar en la gestión del ciclo de vida de su producto farmacéutico.
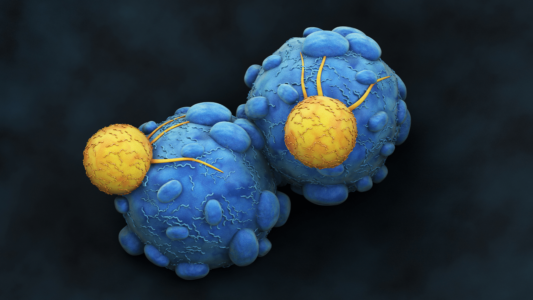
La terapia celular incluye varios ATMP para luchar contra los tumores o restaurar el estado fisiológico de los tejidos dañados. Explórelos aquí.

El 15 de noviembre de 2021, QbD y TRIUM recibieron el certificado Baanbrekende Werkgever ’22 por ser empleadores belgas pioneros que se esfuerzan por poner a las personas en el centro de sus políticas de trabajo híbrido y movilidad.
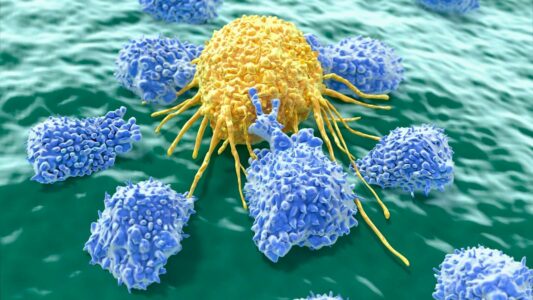
Las células NK, como parte de nuestro sistema inmunitario innato, son muy eficaces para eliminar diferentes tipos de células, incluidas las tumorales. Debido a estas propiedades, resultan muy interesantes como ATMP para la inmunoterapia.
¿Siente curiosidad por el potencial de las células NK y la inmunoterapia basada en ellas? Conozca aquí todo sobre ellos, incluidas las ventajas y los retos.
En la UE, el IVDR sustituirá al IVDD. El plazo de cumplimiento se acerca, así que actúe ahora para obtener el marcado CE de su dispositivo médico IVD a tiempo.

Siga estos pasos antes de lanzar productos combinados de productos sanitarios en la UE, incluida la aplicación del artículo 117 del MDR y la Directiva de la EMA.

Obtenga más información sobre el nuevo enfoque basado en el riesgo para la clasificación de dispositivos de diagnóstico in vitro en virtud del IVDR 2017/746, que sustituye a las directivas obsoletas.
Las células dendríticas desempeñan un papel importante en las inmunoterapias basadas en DC desarrolladas recientemente para el tratamiento del cáncer, las enfermedades autoinmunes y la prevención del rechazo de injertos. Lea todo sobre las células DC y su potencial en este artículo.
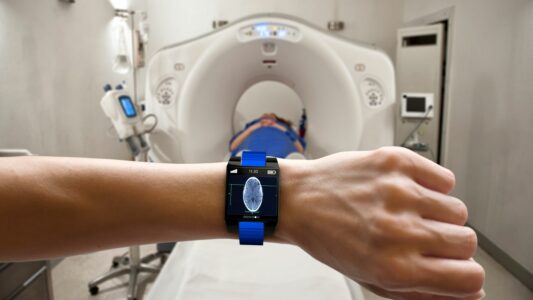
¿Tiene curiosidad por conocer las últimas tendencias del sector de los dispositivos médicos? Obtenga más información sobre los wearables, la IA, las pruebas POC, el IoT y mucho más en esta publicación del blog.
Come to see the QbD Group at stand #3G73 at CPHI Conference in Barcelona. And after the conference…Eat & Connect with lifescience professionals at our QbD’s CPHI Networking Drink.