Existen 6 tipos principales de impactos a considerar para los sistemas computarizados.
Estos deberán de evaluarse tanto en los análisis de riesgos iniciales al sistema como para los posteriores análisis de riesgos (a Requerimientos y durante el mantenimiento del estado validado):
Ejemplos de Impactos BPx:
- Seguridad del Paciente: tienen este tipo de impacto los sistemas que liberan productos o gestionan información para uso del paciente (lote, instrucciones, caducidad), p.ej. HPLC, software de codificadora, etc.
- Calidad del Producto: sistemas con este tipo de impacto participan directamente en la fabricación o en la evaluación de parámetros críticos, p.ej. espectro IR, TOC, PLC de una autoclave, etc.
- Integridad de Datos: Los sistemas ERP, Sistemas de control de Inventarios, Sistemas de Gestión Documental, etc.
- Cumplimiento regulatorio: Sistemas de control del SGC, hojas de cálculo donde se controlen los planes de capacitación o de mantenimiento, bitácoras electrónicas, etc.
- Políticas internas: Sistemas que gestionan la calificación del personal, sistemas de seguridad, etc.
Es importante considerar que un mismo sistema puede tener más de un tipo de los impactos mencionados. En este caso, profundizaremos en los impactos en la integridad de datos.
¿Cómo se pueden ocasionar impactos a la integridad de datos?
Cuando se carece de controles para el uso, archivo, respaldo, restauración, transmisión y modificación de los datos e información que gestiona el sistema.
Un ejemplo es, que, al utilizar un software de control de inventarios en un almacén, algún empleado tenga un error en el movimiento entre almacenes de un producto “X”, solicite a su amigo que está en el área de TI y que se encarga de la gestión de dicho sistema que realice el arreglo del error cometido por el empleado del almacén mediante la modificación del dato, en este caso el sistema es vulnerable y su información no puede ser considerada como integra.
¿Qué es y por qué es importante mantener la integridad de los datos?
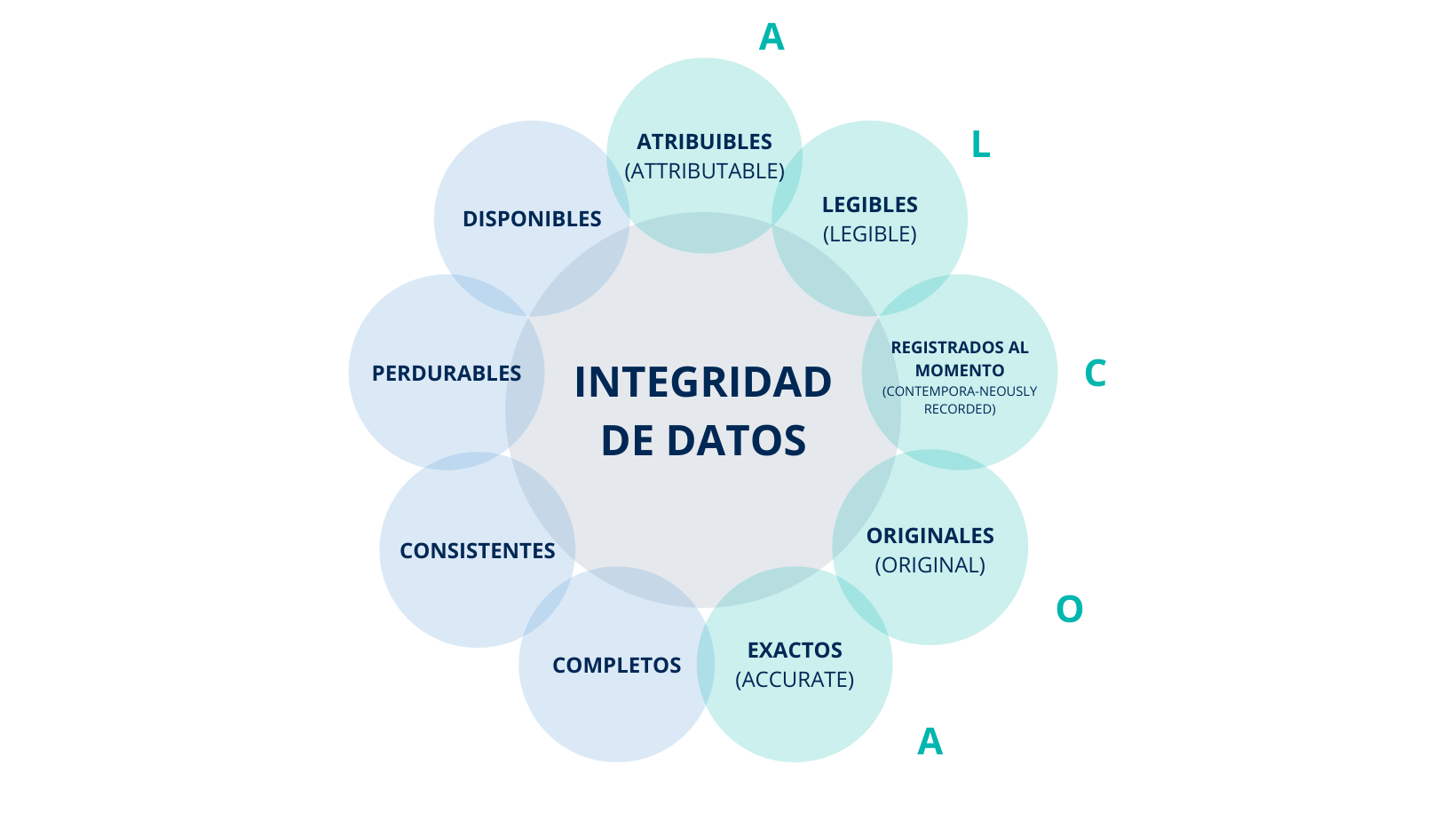
La FDA en su guía “Data Integrity and compliance with cGMP” establece que la integridad de datos se refiere a que los datos deberán permanecer atribuibles, legibles, registrados en el momento, originales (o copias reales) y exactos, los atributos anteriores son mencionados por la FDA bajo el acrónimo ALCOA (Attributable, Legible, Contemporaneously recorded, Original or a true copy, and Accurate) además de completos, consistentes, perdurables y disponibles.
Estos conceptos han sido reproducidos a su vez por otras guías y regulaciones.
Cuando se habla de datos, hay que tener presente que estos forman parte de los Registros gestionados por el sistema.
En el manejo de datos, existe un ciclo de vida el cual, de manera general, contempla las siguientes etapas:
- Generación
- Proceso
- Reporte
- Verificación
- Uso para toma de decisiones
- Almacenamiento
- Descartado al final del periodo de retención
Dentro de estas etapas pueden existir transferencias entre sistemas manuales y/o sistemas IT.
La integridad de datos debe mantenerse cuando los datos gestionados por los sistemas son de relevancia para el cumplimiento de las buenas prácticas, forman parte de la evidencia de cumplimiento ante la agencia reguladora o son críticos para el cumplimiento y medición de los atributos de calidad del producto o para la seguridad del paciente.
Cuando el sistema no es capaz de soportar y mantener la integridad de los datos que gestiona, se genera un riesgo importante, ya que estos datos críticos pueden ser falseados, borrados, divulgados sin autorización, modificados o negados por los emisores.
La gobernanza de los datos permite mantener la integridad de datos.
¡RECUERDA! EN WWW.QBD.DIGITAL TE PODEMOS AYUDAR CON:
Validación de Sistemas Computarizados Validación de Procesos | Validación de Limpieza | Validación de hojas de cálculo | Calificación de Equipos | Data Integrity |
Contáctanos en:
- Norteamérica: (+55) 5516 6646
- Suramérica: (+57) 350-8886031
- Europa: (+34) 655 591 603
¡Únete a nuestra comunidad en redes!

