En el mundo de las Life Sciences circula un sinfín de documentos de conformidad. No es diferente en el caso de los sistemas informáticos. No siempre es tan fácil saber qué necesita su sistema para cumplir la normativa y cómo puede conseguirlo.
Uno de los documentos con los que nos encontramos a menudo es " Software de dispositivos médicos - Parte 2: Validación de software para sistemas de calidad de dispositivos médicos,ISO/TR 80002-2:2017, IDT". Nos referiremos a él como ISO 80002.
Como exige la norma ISO 13485:2016: 4.1.6, 7.5.6, y 7.6 ., este documento se aplica al software utilizado en los sistemas de calidad de productos sanitarios, incluyendo:
- Software utilizado en sistemas de gestión de calidad
- Fabricación
- Prestación de servicios
- Seguimiento y medición de requisitos
Consiste en una lista de normas que el sistema debe cumplir. Pero, ¿qué hacer con una lista de normas y sugerencias vagas? Podría dejar a la gente con más preguntas que respuestas.
Aquí es donde GAMP5 (Good Automated Manufacturing Practice) ha intentado ofrecer una guía práctica para la validación y gestión de los sistemas automatizados utilizados en farmacia.
Esta guía fue publicada por la Sociedad Internacional de Ingeniería Farmacéutica ( ISPE) y se utiliza como referencia internacional para el cumplimiento de la normativa.
Ahora podemos preguntarnos si los sistemas cumplen la norma ISO 80002-2 si seguimos todas las directrices descritas en GAMP5. En este artículo, abordamos esta cuestión, con la esperanza de ampliar sus conocimientos sobre:
- Procesos y entregables requeridos para ISO 80002-2
- Cuáles de estos procesos están incluidos en GAMP5
Hacemos la comparación para que no tengas que hacerlo.
Disfruta de la lectura.
¿Cómo compararemos ISO 80002-2 y GAMP5?
Repasaremos el ciclo de vida de los sistemas informatizados para software no relacionado con productos y los sistemas informatizados utilizados en la industria farmacéutica. La norma ISO 80002 establece que se pueden aplicar muchos modelos de ciclo de vida de desarrollo.
También establece que ninguno de estos modelos será defendido o recomendado. Sin embargo, sí se espera una metodología controlada, que se explica en el documento con bastante detalle. ¿Qué significa esto en la práctica? Seguir las normas del documento.
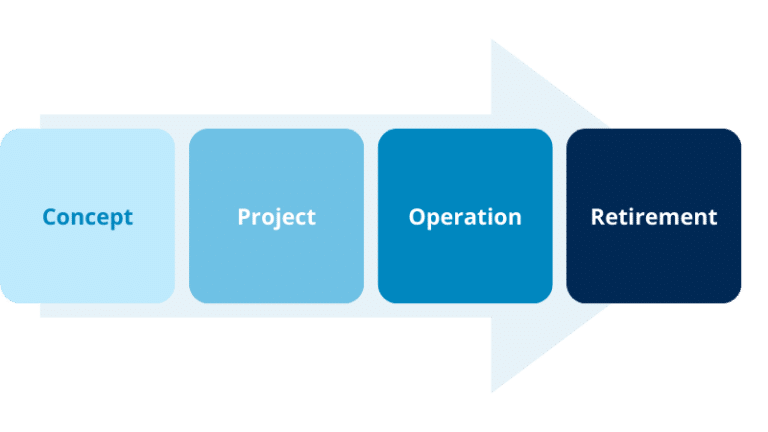
El ciclo de vida de un producto consta de cuatro fases principales:
-
Concepto, en la que se define lo que debe hacer el sistema.
-
Proyecto, en la que se desarrolla y demuestra que la solución funciona correctamente.
-
Operación, en la que se utiliza el sistema validado y se intenta mantenerlo en ese estado.
-
Retirada, cuando se despide del sistema.
Figura 1 - Ciclo de vida de los sistemas informáticos para software no relacionado con productos y sistemas informáticos utilizados en farmacia
Durante este ejercicio, echaremos un vistazo a cada fase y enumeraremos los entregables y actividades requeridos por ISO 80002, y cómo/si GAMP5 trata estos temas.
Procesos de apoyo
Antes de examinar cada fase individualmente, hay algunos procesos necesarios que no son específicos de ninguna fase del ciclo de vida, pero que se aplican de una forma u otra durante cada fase. GAMP5 los enumera como procesos de apoyo. Analicemos los más importantes:
Gestión de riesgos
La norma ISO 80002 establece que debe existir una gestión de riesgos y que debe utilizarse un enfoque basado en los riesgos. También establece que los riesgos asociados al software deben reducirse a un nivel aceptable.
La guía GAMP5 ha incorporado esto en el capítulo 5 y en el apéndice M3. El apéndice explica cómo incorporar la gestión de riesgos de calidad basada en la ciencia en todas las fases del ciclo de vida, y cómo escalar, mitigar y tratar los riesgos residuales:
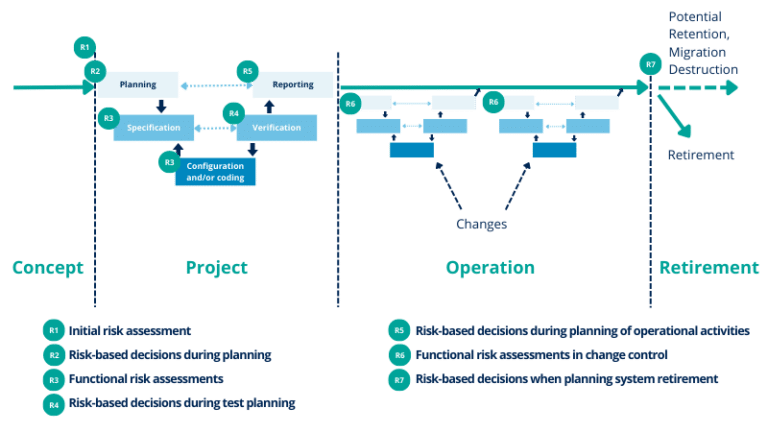
Figura 2- Cómo incorporar la gestión de riesgos de calidad basada en la ciencia en todas las fases del ciclo de vida, y cómo escalar, mitigar y tratar los riesgos residuales según GAMP5, capítulo 5 y apéndice 3.
Trazabilidad
Garantizar la trazabilidad entre todas las actividades no sólo es un requisito de la norma ISO 80002, sino también una forma práctica de **hacer un seguimiento** de lo que se ha hecho y por qué.
¿Qué significa esto? Pues bien, al **vincular** las necesidades de los procesos empresariales con los requisitos, y al vincular éstos con los esfuerzos de verificación y la gestión de riesgos, conseguimos un mapeo.
Este mapeo, a menudo denominado **matriz de trazabilidad**, puede utilizarse para garantizar que todos los requisitos se abordan adecuadamente.
No hay que ver la trazabilidad sólo como algo que debe hacerse **.** **No puedo insistir lo suficiente en lo práctica que resulta una trazabilidad adecuada** a la hora de realizar la gestión de riesgos o las evaluaciones de impacto.
Fases del ciclo de vida
1. Prueba de concepto
La prueba de concepto se conoce como la fase de concepto en GAMP5. En la fase de concepto, todo comienza.
Antes de que se pueda desarrollar o comprar una solución, debe saber qué es lo que usted y sus partes interesadas necesitan y para qué se utilizará la solución (uso previsto). Para registrar estas necesidades, es necesario establecer los requisitos del usuario. Además de eso, es una buena idea empezar a buscar proveedores potenciales. Esto podría ayudarte a tener una idea de lo que ya existe.
A pesar de que la fase de concepto no es formalmente parte del alcance de la norma ISO 80002, conceptos como los requisitos de uso, el propósito y la intención (uso previsto), son requeridos por la norma ISO 80002 y están incluidos y bien explicados en GAMP5.
2. Fase de proyecto
La fase del proyecto es donde se realiza todo el trabajo real para desarrollar la solución, demostrar que funciona correctamente e implementarla.
La fase del proyecto incluye 5 subfases:
- Planificación
- Características técnicas
- Desarrollo: configuración y codificación
- Verificación
- Presentación de informes y publicación
Haremos un punto muerto en algunos de los entregables y actividades requeridas en estas subfases.
Planificación
La planificación debe cubrir todas las actividades, responsabilidades, procedimientos y plazos requeridos. Míralo como una gestión de proyecto s para todo lo que hay que hacer hasta que se pueda utilizar la solución.
Lo que requiere la norma ISO 80002 es que todas las actividades de validación y los entregables se registren en un Plan de Validación. De acuerdo con GAMP5, esta es la responsabilidad del propietario del proceso y debe incluir:
- El alcance del sistema
- Objetivos del proceso de validación
- Principales normativas aplicables
Si es necesario, también se deben revisar los requisitos del usuario. Es muy probable que algunos de ellos necesiten ser ajustados.
Desarrollo: especificación, configuración y codificación
Este paso corresponde a la fase de desarrollo.
Estos pasos dependen en gran medida de sus casos específicos. Es bastante lógico que el software estándar requiera un enfoque diferente al software que será desarrollado completamente por uno mismo.
Antes de desarrollar algo, no sólo hay que saber lo que se va a desarrollar y por qué es importante o necesario, sino también cómo se va a implementar.
Esta es la función de las especificaciones o especificaciones de diseño. Esto es, por supuesto, si vas a desarrollar un sistema nuevo o altamente personalizado.
En esta fase, la solución se construye/adapta/configura/... de acuerdo con las especificaciones y/o requerimientos del usuario.
La norma ISO 80002 no establece cómo debes desarrollar tu software. Mientras cumpla con sus otras reglas, son felices.
Verificación
La verificación es la actividad que se lleva a cabo para confirmar que se han cumplido las especificaciones. Esto se hace mediante pruebas.
La norma ISO 80002 deja las pruebas abiertas a la interpretación. Establece que las pruebas deben basarse en los factores y factores de riesgo y deben proporcionar un nivel adecuado de confianza para demostrar que el software cumple con los requisitos y las especificaciones de diseño. También establece que se deben planificar las actividades de prueba.
GAMP5 también aborda las pruebas desde un punto de vista basado en el riesgo, donde todas las actividades deben planificarse. En el Apéndice D5 se describe cómo se podrían realizar las pruebas de los sistemas computarizados regulados por GxP.
Además, hay en el mercado una guía separada sobre un enfoque basado en el riesgo para las pruebas de los sistemas GxP.
Presentación de informes y publicación
El Informe de Validación es el entregable más conocido durante esta fase. Se trata de un resumen de las actividades realizadas, una lista de cualquier desviación, acciones correctivas abiertas y una declaración de idoneidad para el uso del sistema. La guía GAMP5 marca todas las casillas de verificación necesarias para ISO 80002 para el informe de validación.
Planificación del mantenimiento: La norma ISO 80002 establece que la planificación del mantenimiento durante la fase de desarrollo puede definir cuáles de las actividades operativas se pueden realizar sin afectar a la validación y qué cambios requieren esfuerzos de validación.
En esencia, debes pensar en qué actividades regulares de bajo riesgo se realizarán para mantener el buen funcionamiento del sistema. En GAMP5, esto se integra durante el desarrollo en la subfase de especificación.
Una vez que se cumplen los entregables, puede comenzar la siguiente fase.
¡No olvides celebrar este importante hito con todos tus grupos de interés!
3. Fase de Operación - Fase de Mantenimiento
La fase de operación es donde realmente utilizará el sistema. Con un poco de suerte, esta fase es la más larga de todas las fases hasta ahora.
Entregables ISO 80002
- Gestión del cambio
- Seguimiento periódico
- Gestión de incidencias
- Gestión de la configuración
Durante la fase de operación, el intento es mantener el sistema computarizado en un estado validado. Lo más probable es que, en algún momento durante la fase de operación, se requieran ciertas acciones para mantener el buen rendimiento del sistema automatizado y aún en el estado validado deseado. Aquí es donde la gestión del cambio jugará un papel importante, como se indica en la sección 4.1.4 de la norma ISO 13485. En caso de que estés interesado en la gestión del cambio, lee esta publicación de blog. Para la mayoría de los sistemas, la fase operativa es la fase más larga, así que préstele suficiente atención.
Deben existir revisiones periódicas documentadas y basadas en el riesgo para evaluar el impacto en la seguridad del paciente, la calidad del producto y la integridad de los datos.
En un mundo ideal, no hay problemas. Desafortunadamente, no vivimos en un mundo ideal. Esta es la razón por la que se debe implementar la gestión de incidentes.
Esto no se menciona específicamente en la norma ISO 80002. En su lugar, se refiere a la norma ISO 13485. Este es un ejemplo de cuáles son los problemas al trabajar con documentos ISO. No toda la información se coloca en un solo documento. La norma ISO 13485 describe los incidentes y eventos de la misma manera que GAMP5:
- Gestión de incidentes y problemas
- Proceso de Acción Correctiva y Preventiva (CAPA)
En resumen, los incidentes son efectos reportados en forma de eventos vinculados al sistema, que pueden originarse en cualquier lugar. Estos eventos deben ser categorizados e investigados con el objetivo de lograr una resolución oportuna. ¿Sabías que la palabra "incidente" ni siquiera está en la norma ISO 80002-2?
CAPA es un proceso basado en la causa raíz para investigar, comprender, corregir y prevenir situaciones no deseadas. La prevención se realiza principalmente mediante cambios en los procesos. Muchos incidentes pueden formar parte de una CAPA.
La administración de la configuración debe estar presente. Se menciona como un entregable durante la fase de operación. Podría ser beneficioso establecer este proceso antes, ya que podría ayudar a realizar un seguimiento de las posibles compilaciones o versiones intermedias durante el desarrollo o la codificación en sí. La gestión de la configuración continuará hasta que el sistema se retire.
4. Fase de retiro
En esta fase, el ciclo de vida de su sistema llega a su fin. La forma más fácil es simplemente dejar de usarlo. También aquí, no es tan simple. Existen algunas reglas para garantizar que esto se haga correctamente.
La norma ISO 80002 no proporciona entregables específicos para esta fase. En cambio, afirma que esto depende del tipo de software que se retire y de su uso previsto.
La retirada del sistema se considera un cambio (véase: gestión del cambio), en el que un sistema queda fuera de uso. El impacto de ese cambio es que el sistema ya no está en uso para realizar ciertas tareas o cumplir ciertas funciones.
GAMP5 también considera esto como un cambio y, además, agrega una capa de cómo migrar, archivar y recuperar datos que fueron almacenados y utilizados por el sistema. En la norma ISO 80002 se proporciona una lista de cuestiones a tener en cuenta. Estos deben tenerse en cuenta durante la evaluación de impacto del cambio.
Comparación entre ISO 80002-2 y GAMP5: conclusión
Hemos intentado recopilar los entregables de ISO 80002-2 y si GAMP5 trata estos temas y cómo lo hace. Hemos encontrado que estos dos son muy similares en los temas que manejan. GAMP5 es una guía completa que incluye casi todos los temas de ISO 80002.
Debido a esto, podemos concluir que si tu sistema ha sido (correctamente) configurado de acuerdo con la guía GAMP5, estás cubierto para ISO 80002-2. Además, hay algunos temas que se incluyen en GAMP5, que no son requeridos por ISO 80002.
¿Es el uso de GAMP5 una buena opción para tu software no relacionado con productos?
Esta es probablemente la pregunta más importante. Sin embargo, como ocurre con la mayoría de las respuestas, ésta también empieza con: Bueno, depende...
Algunas personas son algo reacias a trabajar con GAMP5. Entendemos que un libro de casi 400 páginas puede resultar bastante abrumador en lugar de las 84 páginas de ISO 80002-2. Después de hacer esta comparación, podemos concluir que estas casi 5 veces más páginas, no añaden carga de trabajo. Al contrario, una explicación exhaustiva sobre cómo desarrollar y aplicar determinados procesos podría reducir el tiempo.
Para que quede claro, trabajar únicamente con ISO 80002 no es una forma equivocada de hacer las cosas. En nuestra opinión, es mucho más fácil trabajar con la guía GAMP5. Elimina la mayoría de los problemas que se encuentran cuando se trabaja con las normas ISO. Los entregables requeridos para la ISO 80002-2, se reelaboran e incorporan en GAMP5 de una manera más práctica.
Entonces, ¿utilizas ISO 80002 o GAMP5? Como con la mayoría de las cosas en la vida, es una elección. Nosotros preferimos la forma más práctica.
¿Eres nuevo en la validación de sistemas y necesita ayuda para empezar? Nuestros expertos estarán encantados de ayudarte en tus procedimientos para sistemas informáticos, en función de los recursos de que dispongas. No dudes en ponerte en contacto con nosotros si tienes alguna pregunta.
¿Buscas garantizar la conformidad y fiabilidad de tu software?
Desde la gestión de datos hasta la validación del software, nuestras soluciones garantizan el cumplimiento normativo y la eficiencia operativa.
Sobre el autor

Senior Consultant Software Services
Jan Appelmans is a Software Specialist at QbD Group, working across Belgium and the Netherlands. With over a decade of hands-on experience in the IVD industry — including 8 years at Biocartis spanning QA, regulatory documentation, system engineering, and platform analysis — Jan brings a deep understanding of medical device software and compliance from both the manufacturer and consulting side. At QbD Group, he helps life science companies navigate software validation, digital compliance, and the transition to electronic IFU.
QbD Group
¿Listo para acelerar tu proyecto en Life Sciences? Habla con nuestros expertos.
Contacta con un experto →