
Pharma & Biotech
En QbD Group somos expertos en el desarrollo y la producción de productos farmacéuticos.
Apoyo regulatorio completo
Gestión experta del CMC
Apoyo integral en el desarrollo del producto
Nuestra oferta para Pharma en
.jpg)
.jpg)












.jpg)


.jpg)
-1.jpg)
.jpg)
.jpg)

.jpg)
.jpg)




.jpg)


.jpg)


.jpg)

.jpg)


.jpg)

-1.jpg)

-2.jpg)
%20%26%20Responsible%20Person%20(RP)%20Services%20-%20Quality%20Assurance%20-%20QbD%20Group.jpg)
%20%26%20Product%20Quality%20Review%20(PQR)%20%20QbD%20group.jpg)



.png)

.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)



%20-%20Toxicology%20-%20QbD%20Group.jpg)


.jpg)
.jpg)







.jpg)

Retos del sector
En un contexto de costes en aumento, mayor enfoque en los desarrollos globales y operaciones de fabricación, la industria farmacéutica requiere una planificación precisa y un conocimiento profundo de los aspectos normativos, de calidad y clínicos para llevar los medicamentos al mercado.
El ciclo de vida reglamentario de las autorizaciones de comercialización de medicamentos puede ser un desafío que consume muchos recursos. Tras obtener el registro, se deben gestionar numerosas variaciones cada año. Reducir los plazos de comercialización exige un dominio completo de las directrices científicas y normativas de la EMA y la ICH para el desarrollo de medicamentos basados en moléculas pequeñas.
El desarrollo de nuevas moléculas genéricas comienza al principio del ciclo de vida del producto original (en el momento de su lanzamiento al mercado), por lo que es esencial una planificación a largo plazo. Mientras que los genéricos de moléculas pequeñas pueden ser sencillos, los genéricos complejos requieren conocimientos especializados.
QbD Group puede ayudar a los desarrolladores farmacéuticos con la gestión del ciclo de vida completo de sus autorizaciones de comercialización, como garantizar que la sección CMC (Química-Fabricación-Control) del expediente de registro (Módulo 3 del CTD) se ajuste a las expectativas normativas.

Retos del sector
En un contexto de costes en aumento, mayor enfoque en los desarrollos globales y operaciones de fabricación, la industria farmacéutica requiere una planificación precisa y un conocimiento profundo de los aspectos normativos, de calidad y clínicos para llevar los medicamentos al mercado.
El ciclo de vida reglamentario de las autorizaciones de comercialización de medicamentos puede ser un desafío que consume muchos recursos. Tras obtener el registro, se deben gestionar numerosas variaciones cada año. Reducir los plazos de comercialización exige un dominio completo de las directrices científicas y normativas de la EMA y la ICH para el desarrollo de medicamentos basados en moléculas pequeñas.
El desarrollo de nuevas moléculas genéricas comienza al principio del ciclo de vida del producto original (en el momento de su lanzamiento al mercado), por lo que es esencial una planificación a largo plazo. Mientras que los genéricos de moléculas pequeñas pueden ser sencillos, los genéricos complejos requieren conocimientos especializados.
QbD Group puede ayudar a los desarrolladores farmacéuticos con la gestión del ciclo de vida completo de sus autorizaciones de comercialización, como garantizar que la sección CMC (Química-Fabricación-Control) del expediente de registro (Módulo 3 del CTD) se ajuste a las expectativas normativas.
¿Por qué QbD Group?
EXPERTOS EN CIENCIAS DE LA VIDA
En QbD Group, nuestro equipo de Regulatory Affairs tiene la experiencia que necesitas para guiar a tu empresa en el cumplimiento de los requisitos normativos en el desarrollo de moléculas pequeñas y genéricos. Te ayudamos a preparar un expediente de registro completo y listo para presentar a las autoridades competentes.
Además, te acompañamos en todo el proceso de registro, desde la presentación de la solicitud de autorización de comercialización (AC) hasta su concesión, ya sea para medicamentos genéricos o híbridos.
+10 años de experiencia
Asistencia durante todo el ciclo de vida
Presencia mundial
Empresa mejor gestionada

Contacta con nosotros
Contacta hoy mismo con nuestros expertos y descubre cómo en QbD Group podemos ayudarte con tus proyectos de genéricos y moléculas pequeñas. Rellena el formulario y te responderemos lo antes posible para que lleves tus productos al mercado de manera eficiente y cumpliendo con todas las normativas.
Recursos




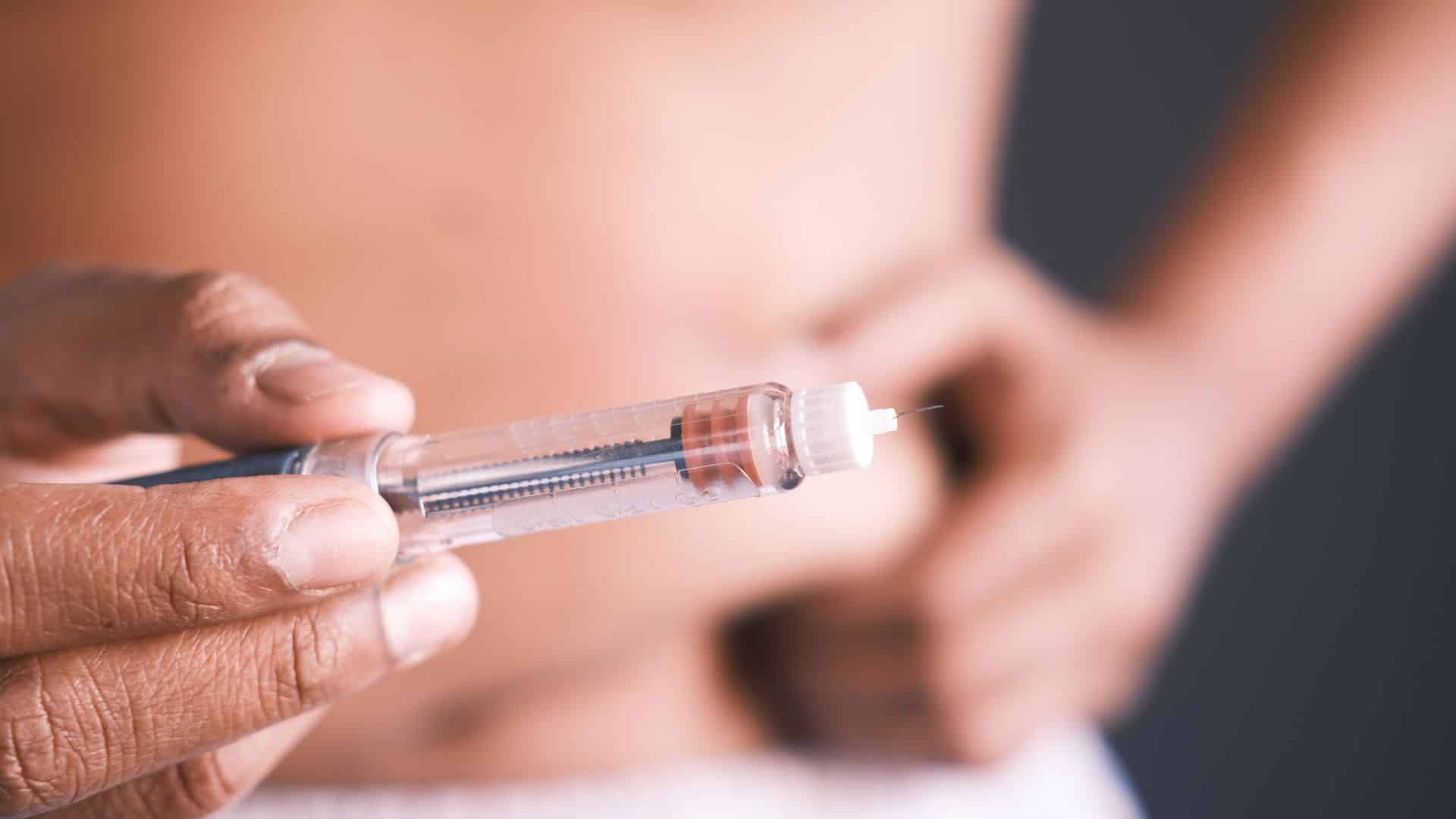
Transformando consultas en insights: el rol estratégico de los Medical Call Centers en Pharma


.jpg)





Guiar la investigación del glioblastoma de la Universidad Católica de Lovaina hacia la clínica con una planificación empresarial precisa










Garantizar el lanzamiento a tiempo: El papel del Grupo QbD en la creación de una línea de producción de medicamentos para la hemofilia
.png)

Revolucionando la farmacovigilancia: una historia de éxito de asociación estratégica e integración sin fisuras
¡Conoce las últimas tendencias en Life Sciences!

Ven a conocernos en los siguientes eventos
mayo
junio
septiembre
octubre
noviembre


Descubre nuestra experiencia en otros sectores
En QbD Group vamos más allá de la industria farmacéutica: somos tu socio de confianza en dispositivos médicos y diagnóstico in vitro. Descubre cómo nuestras soluciones personalizadas pueden impulsar la innovación y garantizar el cumplimiento normativo en estos sectores.






.png?width=109&height=108&name=Pharma%20(2).png)



.jpg)

