Uno de nuestros anteriores artículos del blog se hablaba de las tendencias e innovaciones del sector de los dispositivos médicos.
Desde entonces, se dispone de datos más recientes sobre el número de solicitudes de patentes procedentes de la investigación anual de la Organización Europea de Patentes (OEP). Pueden utilizarse como medida de la innovación en el sector de la tecnología médica y en otros sectores.
En contra de las expectativas de muchos, la industria de la tecnología médica sigue siendo líder, superando a la de la comunicación digital y la informática. Según esta investigación, en 2020 se presentaron 14.295 solicitudes de patentes de tecnología médica [1].
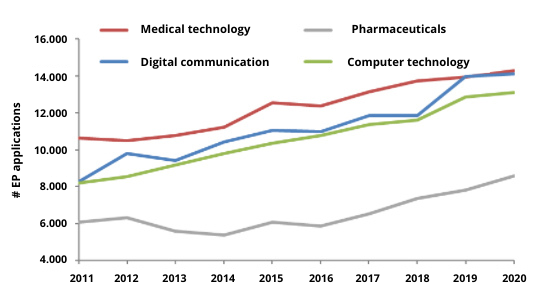
Figura 1 – Nº de solicitudes de PE basadas en datos de la OEP [1]
Cada vez más, los programas informáticos ocupan un lugar central, tanto en los dispositivos médicos como en su entorno. Los acrónimos SaMD (Software as a Medical Device), SiMD (Software in a Medical Device) y MDSW (Medical Device Software) son cada vez más familiares.
Hoy en día, los dispositivos están “conectados” gracias al auge de la Internet de las Cosas (IoT) y sus componentes (smartphones, wearables, servidores en la nube, tecnología de sensores más barata y mejor, big data e IA). La pandemia del virus Covid aceleró aún más esta tendencia de la industria de los dispositivos médicos y exigió servicios sanitarios a distancia.
En esta entrada del blog, profundizamos un poco más en algunas de estas tendencias y tecnologías de la industria de dispositivos médicos y su aplicación a la industria médica.
4 grandes tendencias de la industria de dispositivos médicos
Sensores y wearables
Gracias a la miniaturización y la rentabilidad de la tecnología de sensores, éstos se incorporan a todo tipo de formatos corporales, como parches, relojes o vendas. Estos wearables están promoviendo un uso creciente en la monitorización continua de las condiciones de salud.
Por ejemplo, estos sensores pueden controlar el estado clínico de un paciente y estos datos, a su vez, pueden ser utilizados incluso por un software para determinar la necesidad de una intervención.
Tenga en cuenta que no todos estos dispositivos portátiles pueden clasificarse como productos sanitarios. Depende mucho del uso que se le dé. Piensa en tu reloj inteligente que monitoriza tu ritmo cardíaco para fines relacionados con el fitness o que hace un seguimiento de tu patrón de sueño.
Para este tipo de usos, el fabricante suele afirmar que los resultados no pueden utilizarse para ningún fin clínico. Por lo tanto, no necesita cumplir la normativa sobre productos sanitarios. En caso de que los datos de los sensores se utilicen para la toma de decisiones clínicas, estos dispositivos deben cumplir con la normativa aplicable a los dispositivos médicos.
Inteligencia Artificial (IA)
Uno de los cambios más profundos en la atención sanitaria actual es el uso de dispositivos médicos que incorporan software con Inteligencia Artificial (IA) y Aprendizaje Automático (ML).
Piense en: los glucómetros en el control de la diabetes, y su posibilidad de optimizar la administración de insulina, o los programas informáticos capacitados para detectar arritmias en electrocardiogramas o diagnósticos por imagen.
Sin embargo, la incorporación de estas tecnologías en los dispositivos médicos es también uno de los retos más profundos, no sólo desde el punto de vista técnico, sino también desde el punto de vista normativo.
Esto también es reconocido por la FDA, que recientemente emitió un plan de acción reglamentario .
Todavía faltan orientaciones sobre la aplicación de la normativa europea sobre productos sanitarios a los productos que incorporan estas tecnologías.
Por lo tanto, hemos creado un una entrada de blog separada que profundiza en este tema.
Diagnóstico y pruebas en el punto de atención
En la era del coronavirus, los dispositivos médicos han captado la imaginación del público como nunca antes. Los respiradores y las mascarillas han salvado probablemente miles de vidas. Además, el virus también aceleró la tendencia de los dispositivos médicos a acercar los diagnósticos al paciente, las llamadas pruebas en el punto de atención (POC).
A diferencia de los diagnósticos tradicionales, en los que las muestras del POC se envían a laboratorios centralizados y la gente tiene que esperar horas/días/semanas para obtener los resultados, las pruebas del POC se realizan en la consulta del médico, en la farmacia o incluso en casa.
Las pruebas POC reducen la carga de la logística de las muestras y nos permiten centrarnos en lo que importa, es decir, en permitir un triaje rápido y decisiones de tratamiento clínico.
Para ello, los sistemas de pruebas POC se benefician de las tecnologías descritas anteriormente. Estos dispositivos pueden conectarse a los teléfonos y pueden subir los datos a la nube para que los médicos los revisen o a un software para seguir las tendencias y los brotes de enfermedades infecciosas.
El Internet de las cosas (médicas)
Todas las tecnologías descritas en los apartados anteriores dan lugar a una enorme cantidad de datos. Los dispositivos se están conectando e incluso los dispositivos heredados se están actualizando con capacidades de conectividad.
Todos estos datos se recogen y pueden analizarse, en tiempo real si es necesario, para proporcionar información al paciente, al proveedor de servicios sanitarios o incluso pueden transmitirse a otros dispositivos médicos conectados para su posterior análisis o como entrada.
Se cree que esta conectividad, combinada con la tendencia a los servicios sanitarios a distancia, desempeñará un papel crucial en el futuro de la asistencia sanitaria.
Algunos expertos prevén lo que denominan Internet de los objetos médicos (IoMT) y lo describen como “una infraestructura conectada de dispositivos médicos, aplicaciones de software, sistemas sanitarios y servicios a un sistema informático sanitario centralizado para un análisis de datos más refinado y profundo” [2].
Hoy en día los datos, y obviamente también los datos médicos, son muy valorados. La confidencialidad y la privacidad de estos datos requieren un debate totalmente diferente, pero las empresas de dispositivos médicos, por no hablar de las empresas de tecnología de consumo como Google, Apple y Amazon, están invirtiendo para que esto ocurra:
- El consejero delegado de Apple, Tim Cook, dijo en una ocasión que “si uno se aleja en el futuro, y mira hacia atrás, y se hace la pregunta “¿Cuál ha sido la mayor contribución de Apple a la humanidad? Será la salud.“
- El gigante tecnológico Samsung ha presentado recientemente una patente en la OEP titulada “Método y dispositivo electrónico para la detección de la salud basada en la inteligencia artificial (IA) en la red del Internet de las cosas”.
El concepto general de IoMT y su interpretación exacta pueden parecer todavía algo vagos y futuristas, pero estas tendencias de la industria de dispositivos médicos podrían hacerse realidad antes de lo que se piensa.
Tendencias de la industria de dispositivos médicos: nota final
Es innegable que el futuro de los dispositivos médicos y de la tecnología médica, en general, parece apasionante. Sin embargo, las empresas de dispositivos médicos deben dividir su atención entre una amplia variedad de tareas. No sólo los aspectos técnicos e innovadores de su producto requieren su atención, sino que también los aspectos normativos y de calidad suponen un reto y, en algunos casos, se subestiman.
En virtud de la nueva normativa de la UE sobre productos sanitarios, es decir, el reglamento 2017/745 (MDR), que es aplicable desde el 26 de mayo de 2021, y el reglamento 2017/746 (IVDR), que será aplicable a partir del 16 de mayo de 2022, la clasificación del riesgo y la definición de los requisitos reglamentarios para los productos que contienen programas informáticos y nuevas tecnologías no siempre son sencillas.
Además, se espera que los fabricantes de productos sanitarios sigan las normas y directrices del sector aplicables al software (por ejemplo, ISO13485, ISO 14971, IEC 62304, IEC 82304…), por no hablar de la ciberseguridad.
En QbD, nos enorgullecemos de abordar este tipo de retos. Podemos ayudarle a determinar los requisitos normativos y su estrategia para ajustarse a ellos. Así que si quiere más información, estamos aquí para usted. No dude en ponerse en contacto con nosotros.